Ион - таллий
Cтраница 1
Ионы таллия ( III) в присутствии ионов С1 - и Вг - взаимодействуют с основными красителями, давая малорастворимые соединения. Так, бромидные и хлоридные комплексы таллия образуют с основным красителем родамином Б красно-фиолетовые осадки9, которые экстрагируются органическими растворителями с образованием интенсивно окрашенного в красный цвет экстракта; сам реагент не экстрагируется. Бензольный экстракт соединения НТ1С14 с родамином Б сильно флуоресцирует в ультрафиолетовом свете. [1]
Ионы таллия ( I) обратимо восстанавливаются на капельном ртутном электроде при потенциале около - 0 50 в относительно насыщенного каломельного электрода. [2]
Ион таллия Т1, как и ионы щелочных металлов, бесцветен, мало склонен к образованию комплексных соединений и может замещать ионы щелочных металлов в квасцах. Гидроокиси и карбонаты щелочных металлов и таллия растворяются в воде, их водные растворы имеют сильно щелочную реакцию. Азиды щелочных металлов и таллия являются взрывчатыми веществами. Многие из солей таллия ( TiN03, Т1СЮ3, Т1СЮ4, Т12Сг04 и другие) изоморфны с соответствующими солями калия. Большинство соединений таллия, как и соединений рубидия и серебра, осаждаются в виде безводных солей. [3]
Ионы таллия ( I) обратимо восстанавливаются на капельном ртутном электроде при потенциале около - 0 50 в относительно насыщенного каломельного электрода. Потенциал полуволны не зависит от состава основного электролита. Как на фоне NH4OH, так и на фоне НС1 высота волны пропорциональна концентрации Т1 - ионов в растворе, В аммиачной среде Т11 в отсутствие ионов меди хорошо определяется в металлическом кадмии и его солях. На фоне хлористоводородной кислоты потенциалы полуволн Tl1, Sn11 и РЬП одинаковы. Для разделения волн Sn и Т1 вводят тартрат, подавляющий волну олова, а для разделения волн РЬ и Т1 вводят комплексон III, смещающий в слабокислой среде потенциал полуволны РЬ в сторону более отрицательных значений ( - iti е)) что может быть использовано также при определении TF в свинце. [4]
Ионы таллия ( I) обратимо восстанавливаются на капельном ртутном электроде при потенциале около - 0 50 В относительно насыщенного каломельного электрода. Потенциал полуволны не зависит от состава основного электролита фона. Как на фоне NH3 так и на фоне НС1, высота волны пропорциональна концентрации Т1 - ионов в растворе. В аммиачной среде Т11 в отсутствие ионов меди хорошо определяется в металлическом кадмии и его солях. На фо е хлористоводородной кислоты потенциалы полуволн Tl1, Sn11 и РЬП одинаковы. Для разделения волн Sn11 и Т11 вводят тартрат, подавл-яющий волну олова, а для разделения волн РЬ11 и Т11 вводят ЭДТА, смещающий в слабокислой среде потенциал полуволны РЬП в сторону более отрицательных значений ( - 1 1В), что может быть использовано также при определении Т11 в свинце. В этих условиях медь восстанавливается при потенциале - 0 3 В. Полярографическое определение обычно проводят методом добавок после выделения таллия экстракционным методом. [5]
Ионы таллия ( I) легко восстанавливаются на ртутном электроде из кислых, нейтральных и слабощелочных растворов. Чаще всего для хронопотенцио-метрического определения таллия применяются нейтральные растворы 1 М KN03 [20], 0 1 М K. Катодные и анодные хронопотенциограммы таллия ( I) четко выражены. После внесения поправки на омическое падение потенциала получены следующие значения qt / 4 ( нас. [6]
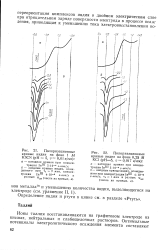 |
Поляризационные кривые индия на фоне 1 М KSCN ( рН 5, v 0 01 в / сек. [7] |
Ионы таллия восстанавливаются на графитовом электроде из кислых, нейтральных и слабощелочных растворов. [8]
Ионы таллия ( III) также осаждаются в виде иодида, но при этом происходит выделение иода. [9]
Ион таллия в условиях выполнения реакции обладает собственной люминесценцией, цвет которой зависит от концентрации; смешиваясь со свечением, обусловленным наличием олова, люминесценция приобретает почти чисто белый цвет. Если таллия мало, то его мешающее действие может быть устранено проведением наблюдения в ультрафиолетовых лучах с длиной волны 365 ммк; в этом случае свечение таллия сильно ослаблено, а цвет люминесценции, обусловленной наличием олова, изменяется от олотисто-желтого до зеленовато-желтого. [10]
Ион таллия дает хорошо выраженные волны практически во всех обычных индифферентных электролитах, и так как он не проявляет заметных тенденций к комплексообразова-нию, то его потенциалы полуволн меняются не очень сильно в различных фонах. [11]
Ион таллия взаимодействует со многими веществами, применяющимися для открытия ионов цезия и рубидия. Он образует еще более трудно растворимые хлороплатинат и кобальтгексани-трит. [12]
Ионы однозарядного таллия Т1 и двухзарядного свинца РЬ2 имеют заряд на две единицы ниже номера групп, к которым они относятся. Это объясняется проявлянием эффекта инертной пары. Эффект инертной пары обусловлен сопротивлением пары 52-элект-ронов, составляющих внешний подуровень, к отщеплению или участию в образовании ковалентной связи. Так, ртуть трудно окисляет ся до двухзарядной, вероятно, потому, что содержит инертную пару б52 - электронов, которая слабо экранируется 4 / - уровнем и потому прочно удерживается ядром атома. [13]
Ионы однозарядного таллия Т1 и двухзарядного свинца РЬ2 имеют заряд на две единицы ниже номера групп, к которым они относятся. Это объясняется проявлением эффекта инертной пары. Эффект инертной пары обусловлен сопротивлением пары s электронов, составляющих внешний подуровень, к отщеплению или участию в образовании ковалентной связи. Так, ртуть трудно окисляется до двухзарядной, вероятно, потому, что содержит инертную пару 6 2-электронов, которая слабо экранируется 4 / - уровнем и потому прочно удерживается ядром атома. [14]
Если ионы таллия имеют заряд ге, то на каждый избыточный по сравнению с составом Т12Те атом Т1 приходится z электронов в зоне проводимости. [15]
Страницы: 1 2 3 4