Ион - таллий
Cтраница 3
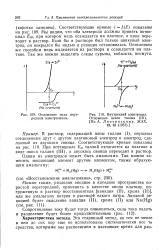 |
Отложение меди внутренним электролизом.| Внутренний электролиз. [31] |
В раствор, содержащий ионы таллия ( I), опущены соединенные друг с другом платиновый электрод и электрод, сделанный из двуокиси свинца. При потенциале Еж таллий отлагается на платине в виде окиси таллия ( III), а двуокись свинца переходит в раствор. [32]
В присутствии большого количества ионов таллия нужно осадить ионы меди и таллия сульфидом натрия и затем растворить сульфид таллия в подходящей мине ральной кислоте, принимая во внимание, что сульфид меди хорошо растворяется только при нагревании с азотной кислотой. Если ионов таллия мало, то лучше осадить медь на платине методом внутреннего электролиза, используя в качестве катода платину, а для анода - никель. [33]
Ионы церия мешают обнаружению ионов таллия, и поэтому их предварительнр удаляют при помощи раствора щелочи. [34]
Уайт [179] предлагает для открытия иона таллия люминесцентную реакцию с водным раствором хлорида калия. Люминесценция возбуждается коротковолновыми ультрафиолетовыми лучами. [35]
При малом содержании ртути можно открыть ионы таллия, предварительно удалив ртуть нагреванием, либо выделив ее на платине в паре платина - никель совместно с медью и свинцом. [36]
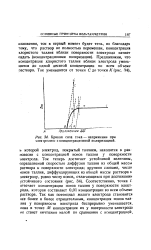 |
Кривая сила тока - напряжение при электролизе с концентрационной поляризацией. [37] |
Соответственно, точка / отвечает концентрации ионов таллия у поверхности электрода, которая составляет 0 01 концентрации во всем объеме раствора. [38]
При введении в раствор иодида калия иона таллия ( I) и последующем высушивании образующиеся кристаллы иодида калия люминесцируют зеленым светом под действием ультрафиолетовых лучей с длиной волны 254 - 313 ммк. Такую же люминесценцию обнаруживают хлорид и бромид калия, но интенсивность свечения их слабее. Цвет люминесценции бромида калия - желтый, а хлорида - желто-зеленый. [39]
Избыток родамина С не мешает определению ионов таллия, так как он не переходит в бензольный слой. [40]
В, какова должна быть концентрация иона таллия в правостороннем полуэлементе. [41]
Если добавленный электролит не содержит ни ионов таллия, ни ионов хлора, то средняя ионная концентрация совпадает с молярной концентрацией хлористого таллия в насыщенном растворе, так как в этом случае сТ1 и ссг равны концентрации соли. Если же в растворе присутствует другая соль таллия или какой-либо хлорид, наличие этих ионов следует учесть. [42]
Полярографическому определению меди в рудах мешают: ионы таллия, потенциал восстановления которого совпадает с потенциалом восстановления меди, что вызывает завышение результатов ее определения; сравнительно высокие содержания кобальта, двухвалентные ионы которого окисляются в щелочной аммиачной среде кислородом воздуха до трехвалентных, восстанавливающихся затем на капельном ртутном электроде при потенциале, более положительном, чем ионы меди; наконец, высокие содержания железа, которое, выпадая из аммиачной среды в форме гидроокиси, может заметно адсорбировать ионы меди. Особенно существенно мешающее влияние железа, когда осадок гидроокиси занимает более половины объема конечного раствора. [43]
С другой стороны, некоторые реакции на ион таллия характерны для иона серебра. Так, подобно серебру, таллий дает трудно растворимые галоидные соли. [44]
 |
Принципиальная схема таллиевого кпслородо-мера типа АК-300. [45] |
Страницы: 1 2 3 4