Ион - тантал
Cтраница 1
Ионы тантала Та5 в щелочной среде реакции не мешают. Ионы титана ( IV) реагируют точно так же и поэтому должны быть предварительно удалены. [1]
Ионы тантала при этих условиях остаются в водной фазе. [2]
Нейтрализованные электронами ионы тантала могут рассматриваться как атомы тантала, расположенные на тех же местах, где находились ионы тантала. [4]
 |
Схема р - n - пере-хода. [5] |
Согласно их представлениям, избыток ионов тантала в оксидном слое сообщает ему электронную электропроводность. Двуокись марганца, также электронный полупроводник, играет двоякую роль: во-первых, как указано выше, является источником кислорода, который восстанавливает диэлектрик в порах и по местам дефектов в оксидном слое, и, во-вторых, создает на поверхности оксидного слоя тонкую пленку из адсорбированных отрицательных ионов кислорода, определяющих дырочную проводимость в этом слое. [6]
Окисный слой образуется в результате диффузии ионов тантала в тонкую окисную пленку, всегда присутствующую на поверхности раздела фаз. Структуру запирающего слоя электрохимически можно представить как анод на границе металл [ окисел и катод на границе окисел электролит, а окисный слой - как биполярный электрод, на котором происходит реакция между ионами тантала, диффундирующими через окисную пленку, и адсорбированными ионами кислорода. [7]
 |
Схема распределения. [8] |
Тантал не растворяется в электролите, вследствие чего ионы тантала и кислорода накапливаются в двойном слое, пока заряды не создадут потенциала, достаточного для простейшей реакции - образования окиси тантала. Другая возможная реакция - разряд ионов кислорода и выделение кислорода - не происходит при нормальной формовке. Кислород на границе оксидный слбй-электролит выделяется только при пробое оксидного слоя. Очевидно, что окисление тантала происходит при з-начениях потенциала, лежащих между статическим потенциалом тантала в электролите и потенциалом, необходимым для разряда кислорода на оксидном слое в том же электролите. Этот интервал составляет приблизительно 2 в. Однако формовка тантала идет при значительно более высоких потенциалах без разряда ионов кислорода на оксидном слое. Для объяснения этого явления Хэринг рассматривает оксидный слой как своеобразную электролитическую ячейку, в которой тантал действует как анод, адсорбированный на оксидном слое, кислород - как катод, и окись тантала - как электролит. Следует заметить, что во время формовки граница раздела оксидный слой-электролит действует, как катод для ячейки, в которой окись тантала служит электролитом, и как анод водной электролитической ячейки, представляя собой биполярный электрод. [9]
Ионы ниобия ( V), в отличие от ионов тантала, восстанавливаются на ртутном электроде в растворах неорганических кислот, а также в растворах, содержащих органические адденды, давая каталитические волны. [10]
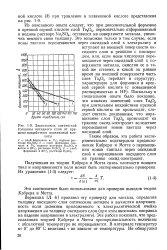 |
Зависимость оптической толщины оксидного слоя от времени воздействия плавиковой кислоты. [11] |
Таким образом, эта работа экспериментально подтвердила предположение Кабрера и Мотта о перемещении ионов тантала через оксидный слой и наращивании оксидного слоя на границе оксид - электролит. [12]
Нейтрализованные электронами ионы тантала могут рассматриваться как атомы тантала, расположенные на тех же местах, где находились ионы тантала. [13]
В слабощелочной среде, напротив, ионы ниобия образуют окрашенное соединение оранжевого цвета24, в то время как ионы тантала окрашивания не дают. [14]
Эти соли не только сходны по своим свойствам, но также способны давать непрерывный ряд смешанных кристаллов, в которых ионы ниобия замещаются на ионы тантала и наоборот. [15]
Страницы: 1 2 3
