Ион - трехвалентный хром
Cтраница 1
Ион трехвалентного хрома можно окислить до хромат - или бихромат-иона действием сильного окислителя, такого, как перекись натрия в щелочном растворе. [1]
Ион трехвалентного хрома Сг3 в отличие от иона Fe2 m окисляется азотной кислотой. [2]
Ион трехвалентного хрома при таких условиях не дает волны. [3]
Восстановление иона трехвалентного хрома проводится в редукторе Джонса. Это избавляет от необходимости фильтровать раствор двухлористого хрома. Редуктор может служить для целой серии опытов, не требуя повторного наполнения цинком. Раствор двухлористого хрома поступает из редуктора в раствор уксуснокислого натрия; таким образом достигается полное использование всей соли хрома. Отделение осадка, образующегося в реакционной колбе Г, от маточного осадка, производится в данном приборе таким образом, что возможность окисления получаемого вещества исключается. [4]
В ионе трехвалентного хрома, имеющем шесть молекул воды, на каждой d - орбитали, обладающей низкой энергией, находится один электрон. Расчет величины этой энергии [73] указывает на то, что о. [5]
Накапливающиеся в растворе ионы трехвалентного хрома могут быть переведены в шестивалентные анодным окислением с использованием свинцового анода и стального катода. [6]
В таком количестве ионы трехвалентного хрома благоприятно влияют на процесс осаждения покрытия. Содержание трехвалентного хрома ( Сг) контролируют анализом не реже одного раза в декаду. В случае излишнего накопления трехвалентного хрома ванну корректируют путем проработки электролита током при большой поверхности анодов и минимальной поверхности катодов. При этом содержание трехвалентных ионов уменьшается в результате окисления их на аноде до шестивалентных. [7]
Аналогично происходит окисление ионов трехвалентного хрома в бихромат-ионы в сернокислой или азотнокислой среде при действии КМпО, или других сильных окислителей. [8]
Дальнейшим осложнением реакций замещения шестиводного иона трехвалентного хрома в щелочных или нейтральных растворах является образование полиядерных комплексов через кислородные мостики. [9]
Дальнейшим осложнением реакций замещения шестиводного иона трехвалентного хрома в щелочных или нейтральных растворах является образование полиядерных комплексов через кислородные мостики. [10]
В то же время добавка ионов трехвалентного хрома снижает проводимость и увеличивает энергию активации каталитической реакции. Эти наблюдения согласуются с заключениями о том, что скорость процесса окисления окиси углерода определяется стадией образования положительных ионов на поверхности окисла никеля - полупроводника р-типа. [11]
При титровании растворами солей двухвалентного хрома образуются интенсивноокрашенные ионы трехвалентного хрома, что иногда затрудняет применение химических индикаторов для установления конечной точки титрования. [12]
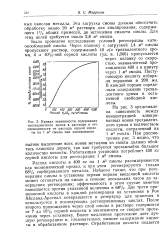 |
Кривая зависимости содержания трехвалентного хрома в растворе и его проводимости от расхода серной кислоты на 1 м3 смолы при элюировании. [13] |
На рис. 3 представлена зависимость между концентрацией элюиро-ванных ионов трехвалентного хрома и количеством кислоты, потраченной на 1 MZ смолы. [14]
NN - ( или - МОг); ион трехвалентного хрома немедленно реагирует с новой молекулой реагента, образуя циклическую соль ( комплекс), раствор которой в кислой среде обладает интенсивной окраской. [15]
Страницы: 1 2 3 4