Ион - трехвалентный хром
Cтраница 3
Для регенерации отработанных растворов хромовой кислоты, использованных для целей органического синтеза, применяется электрохимический способ, при котором ионы трехвалентного хрома анодно окисляются до шестивалентного хрома. Анодное пространство ванны отделено от катодного диафрагмой. Регенерируемый раствор непрерывно пропускается сначала через катодное ( с экранированным катодом), а затем через анодное отделение ванны. [31]
Выход по току для металлического хрома не превышает 30 %, так как значительная часть тока идет на восстановление ионов трехвалентного хрома до двухвалентного. [32]
Наши кинетические данные находятся в интересном соответствии с взглядами Петрова [3] и Кольтгофа и Лайтинена [4], показавших, что ионы трехвалентного хрома не оказывают влияния на окислительно-восстановительный потенциал хроматной системы. [34]
Гидроокись хрома Сг ( ОН) 3 образуется в виде серовато-зеленого хлопьевидного осадка при добавлении гидроокиси аммония или гидроокиси натрия к раствору, содержащему ионы трехвалентного хрома. Осадок растворяется в избытке гидроокиси натрия. [35]
 |
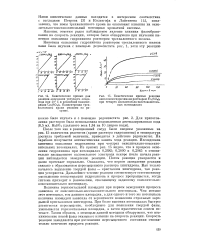
В Условия электрополировки металлов. [36] |
В процессе эксплуатации состав полирующего электролита изменяется: а) уменьшается содержание воды вследствие испарения; б) хромовый ангидрид восстанавливается, в растворе появляются ионы трехвалентного хрома; в) в растворе накапливаются соли металлов; г) концентрация свободных ортофосфорной и серной кислот уменьшается. Происходит увеличение вязкости и уменьшение электропроводности электролита, качество полировки ухудшается. [37]
Красная свинцовая руда представляет собой хромат свинца РЬСгО, Хромистый же железняк FeCr2O4 - это минерал, изоморфный с магнитным железняком, от которого он отличается лишь заменой ионов трехвалентного железа на ионы трехвалентного хрома. [38]
По растворении навески к раствору добавляют 30 мл хлорной кислоты и выпаривают до выделения обильн ( ых паров ее. При этом ион трехвалентного хрома окисляется до иона СгО - о чем свидетельствует выделение солей кирпично-красного цвета. [39]
По причинам, которые вскоре станут ясными, трудно установить определенную зависимость между выходом по току при анодном окислении и материалом электрода. При превращении ионов трехвалентного хрома в хромат-ионы и окислении иодата в периодат, когда окисление вызывается кислородом в активной форме или окислом металла, служащего анодом, наибольшие выходы по току получаются в случае анодов из перекиси свинца и платинированной платины. [40]
Предположим, что ион трехвалентного хрома, Сг3 имеет шесть доступных по энергии орбиталей, 3rfZ2, 3dxz - tft, 4s, 4px, 4py и 4р2, и что линейные комбинации этих атомных орбиталей дают шесть эквивалентных гибридных г / 2 р3 - орбиталей. [41]
При этом йод окисляется в йодат. Ионы шестивалентного хрома восстанавливаются в ионы трехвалентного хрома, что видно по зеленой окраске раствора. Надо добавить столько щавелевой кислоты, чтобы весь хром перешел в трехвалентную форму. Затем в приемник перегонной установки заливают 50 мл 5 % - ного раствора NaHCO3 и отгоняют йод. [42]
При титровании растворами солей двухвалентного хрома индуцированные реакции наблюдаются сравнительно редко. Ионы двухвалентного хрома переходят в ионы трехвалентного хрома, минуя какие-либо промежуточные стадии. Протекание индуцированных реакций отмечено [31] при восстановлении бихромата калия в среде соляной или серной кислоты раствором сульфата двухвалентного хрома. [43]
Интересно, что 1 2-диаминоциклогексантетрауксусная кислота ( комплексен IV) ведет себя по-другому. Этот реактив образует комплексные соединения с хромом значительно медленнее, чем происходит упомянутая гидратация ионов трехвалентного хрома. Поэтому растворы после восстановления хроматов и оттитровы-вания йода в присутствии комплексона IV имеют чисто зеленую окраску. [44]
Метод бихроматометрии основан на применении раствора бихромата калия К2Сг2О7 в качестве рабочего раствора. В кислой среде ионы Ст2Ог - являются сильными окислителями, восстанавливающимися в присутствии восстановителей до ионов трехвалентного хрома. [45]
Страницы: 1 2 3 4