Ион - циан
Cтраница 2
ТТиастидм могут присутствовать в воде в виде цианистоводородной кислоты, ионов циана и комплексных соединений циана. Они могут быть определены по ИСО 6703 в виде общего цианида и цианида, легко выделяемого в свободном состоянии. Если соединения циана хлорированы, то получается хлористый циан ( C1CN), который определяют по отдельной методике. [16]
Цианиды могут присутствовать в воде в виде синильной кислоты, ионов циана и комплексных соединений циана. Они могут быть определены по И СО 6703 в виде общего цианида и цианида, легко выделяемого в свободном состоянии. Если соединения циана хлорированы, то получается хлористый циан ( C1CN), который определяют по отдельной методике. [17]
Как видно, наиболее прочную связь ион серебра образует с ионами циана. Ионы брома связываются гораздо слабее, но все же несколько прочнее, чем ионы хлора. Совсем слабо ионом серебра связываются ацетат-ионы, и, как показывают расчеты, в растворах солей диацетато-сере-бра ( 1) свободных ионов серебра и ацетат-ионов больше, чем комплексных ионов. [18]
Сплавление какого-либо вещества с металлическим натрием применяется для обнаружения в веществе ионов циана, серы, галогенов. При этом легко образуются цианид натрия, сульфид натрия и соединение натрия с галогеном, которые просто открыть любой качественной реакцией. [19]
Однако ввиду того, что в диффузионном слое в процессе электролиза концентрация ионов циана увеличивается, понижение их концентрации вследствие отталкивающего влияния отрицательного заряда поверхности катода может иметь место лишь в двойном электрическом слое. [20]
Следует, однако, отметить, что по вопросу о специфической адсорбции ионов циана в литературе высказываются противоречивые мнения. Так, например, одни исследователи [3, 61] считают, что эти ионы обладают повышенной поверхностной адсорбцией. Между тем, результаты исследований, проведенных Балашовой [286], показывают, что при измерении поверхностного натяжения на границе раствор цианистого калия - воздух, в зависимости от концентрации поверхностно-активных веществ, получаются такие же изотермы адсорбции, как и в растворах сульфатов. На основании этих данных автор делает вывод, что ионы циана повышенной поверхностной адсорбцией не обладают. Однако данный вывод, ло-видимому, не может быть распространен на адсорбцию этих ионов на поверхности различных металлов без дополнительных исследований. [21]
В смеси с солями нелетучих кислот, которые могут мешать при непосредственном определении иона циана, цианистый водород отгоняют в присутствии серной кислоты, улавливают в щелочи и применяют затем один из весовых аналитических методов для его определения. Вместо дестилляции можно легко улетучивающийся цианистый водород также отогнать из подкисленного раствора при помощи струи воздуха или газа. [22]
Различные результаты при действии KCN и AgCN можно объяснить тем, что цианиды щелочных металлов содержат ионы циана CN -, а цианид серебра - ковалентносвязанные атомы серебра. [23]
Различные результаты при действии KCN и AgCN можно объяснить тем, что цианиды щелочных металлов содержат ионы циана CN -, а цианид серебра - ковалептносвязанные атомы серебра. [24]
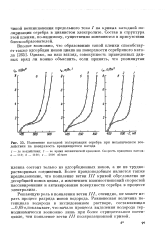 |
Изменение катодной поляризации серебра при механическом воздействии на поверхность вращающегося катода. [25] |
Более правдоподобным является также предположение, что появление ветви / / / кривой обусловлено не десорбцией ионов циана, а изменением взаимоотношений скоростей пассивирования и активирования поверхности серебра в процессе электролиза. [26]
В литературе [4, 23] высказывается мнение, что причиной повышения концентрации свободных ионов металла у поверхности катода является миграция ионов циана под действием электрического поля. Это должно привести к повышению степени диссоциации комплексных анионов и тем самым к увеличению концентрации свободных ионов металла. Однако сторонники этой точки зрения не указывают, на каком расстоянии от поверхности катода такое явление будет иметь место. Между тем известно [24], что в диффузионном слое в процессе электролиза концентрация ли-гандов не уменьшается, а увеличивается. Поэтому понижение концентрации ионов циана можно ожидать только в двойном электрическом слое и лишь в том случае, когда поверхность катода имеет отрицательный заряд. Однако и при этих условиях повышению концентрации свободных ионов металла у поверхности катода должно препятствовать увеличение концентрации посторонних неорганических катионов в двойном слое в процессе электролиза. [27]
Нуклеофилышми реагентами, приносящими пару электронов для образования связи, являются, напр, ион гидроксила, ион галогена, ион циана, аммиак и др. Электрофильными реагентами, стремящимися заполнить электронную оболочку одним или двумя посторонними электронами, являются, напр. [28]
Этот процесс должен идти легко, так как константа нестойкости, отвечающая присоединению первого иона циана к иону платины, на много порядков меньше, чем константа, отвечающая присоединению четвертого иона циана. Получается, что ионы [ PtCl4 ] 2 - или их аналоги должны играть роль своеобразного коллектора появляющихся в растворе ионов, более прочно связывающихся с платиной, чем хлор. [29]
Так, Si ( IV) или P ( V) дают устойчивые и характерные гексацидо-комплексы с ионами фтора, но не дают соответствующих комплексов ни с ионами других галогенов, ни с ионами циана или родана. Алюминий ( III) легко образует ионы A1F63 -, но не дает подобного типа комплексов с другими галогенами. Дает характерных комплексов шестерного типа с ионом циана. Железо ( III) дает прочные гексацидо-комплексы с ионами фтора и с ионами циана или родана, но для него не характерны гексацидо-комплексы с ионами хлора, брома или иода. Золото ( III) в большинстве образуемых им комплексов типа двойных солей показывает к. Подобного же рода гексанитратосоли характерны для ряда редкоземельных элементов. [30]
Страницы: 1 2 3 4