Ион - галлий
Cтраница 2
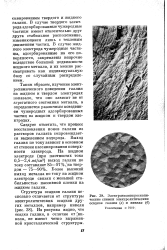 |
Электронномикроскопи-ческие снимки электролитических осадков галлия ( а и никеля ( б. [16] |
Следует отметить, что процесс восстановления ионов галлия из растворов галлата сопровождается выделением водорода. Выход галлия по току зависит в основном от степени пассивирования поверхности электрода. Более высокий выход металла по току на жидком электроде связан с меньшей стабильностью пассивной пленки на жидком галлии. [17]
Задачей настоящей работы является обнаружение образования ионов галлия промежуточной валентности при электрохимическом процессе окисления его с целью непосредственного доказательства стадийного протекания этого процесса. [18]
Последнее обусловливает возможность замещения ионов алюминия ионами галлия в кристаллической решетке основных промышленных минералов алюминия - боксита и нефелина. [19]
Ионы бора и алюминия сильно отличаются от ионов галлия, индия и таллия, хотя вместе они составляют подгруппу IIIA. В ( ОН) 3 проявляет кислые свойства, А. ОН) 3-амфотерное соединение и согласно правилу увеличения основных свойств в направлении сверху вниз ( вследствие увеличения радиусов ионов) следовало бы ожидать увеличения основных свойств у остальных гидроокисей элементов этой подгруппы. ОН) 3 основные свойства выражены слабо. Наружные оболочки ионов бора и алюминия напоминают оболочки благородных газов, а наружные оболочки ионов галлия и других элементов этой подгруппы обладают восемнадцатиэлектронной структурой. [20]
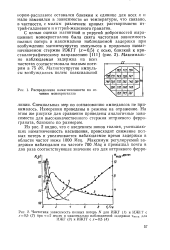 |
Распределение намагниченности по сечению монокристалла.| Частотная зависимость полных потерь N для ИЖГ ( / и ИЖГГ с. [21] |
Из рис. 2 видно, что с введением ионов галлия, уменьшающих намагниченность насыщения, происходит снижение полных потерь и увеличивается наблюдаемое время задержки в области частот ниже 1000 Мгц. [22]
Из сказанного следует, что вопрос о взаимодействии ионов галлия с K4 [ Fe ( CN) 6 ] изучен недостаточно; полностью отсутствуют данные о взаимодействии ионов галлия с ферроцианидами других щелочных металлов. В настоящей работе изучено взаимодействие ионов галлия с ферроцианидами лития, натрия и калия методом физико-химического анализа с целью использования полученных данных для аналитического определения галлия. [23]
Наличие данных о структуре реагирующей частицы стильбазо и состоянии иона галлия позволяет высказать предположение о строении внутрикомплексного соединения, образующегося в данных условиях. [24]
Купферрон - аммонийная соль нитрозофенилгидроксиламина - осаждает из кислых растворов ионы галлия, железа, меди, титана, молибдена, ванадия и многих других металлов, но не осаждает алюминия. Алюминий только захватывается осадком. [25]
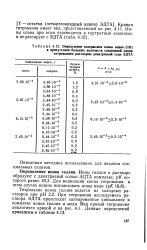 |
Определение содержания ионов индия ( III. [26] |
При титровании исследуемого раствора ЭДТА происходит одновременное связывание в комплекс ионов галлия и меди. [27]
Солохромовые красители ( красный и черный) [116, 119] образуют с ионами галлия комплмсные соединения, которые люминесцируют красным светом. [28]
Резорцин ( л - диоксибензол) в аммиачном растворе дает с ионами галлия сине-фиолетовое окрашивание ( 1057 ], интенсивность которого зависит не от количества галлия, а от количества резорцина. [29]
Азосоединения, содержащие две ОН-группы в ортоположе-нии к азогруппе, взаимодействуют с ионами галлия с образованием окрашенных, а в ряде случаев и флуоресцирующих соединений. Окси-4 - суль-фонафталиназонафталин вызывает в растворах солей галлия оранжевую флуоресценцию в ультрафиолетовом свете. Аналогично реагирует люмогаллион, который применяется для флуо-риметрического определения галлия ( см. стр. [30]
Страницы: 1 2 3 4