Ион - галлий
Cтраница 3
Галлисн ( 0 01 % - ный водный раствор) образует с ионами галлия в слабокислой среде окрашенное в голубой цвет соединение. Максимум свето-поглощения раствора находится при 600 ммк. Чувствительность обнаружения при рН 3 2 составляет 0 2 мкг Ga в 5 мл раствора. [31]
Готовились серии растворов, содержащие 0 5 и 0 05 мкг / мл ионов галлия и различные количества морина. При содержании - галлия 0 5 мкг / мл, рН 3 5 и соотношении [ Ga ]: [ Морин ] 1: 2 прибавление буферного ацетатного раствора вызывает уменьшение интенсивности люминесценции. [32]
Сульфонафтолазорезорцин [58-60] в растворах с рН 3 0 - 3 5 образует с ионами галлия комплексное соединение, люминес-цирующее при облучении ультрафиолетовыми лучами оранжевым светом. [33]
Разница же между структурами (3.51) и (3.48) более значительная, поскольку в соседних четырех-слойных элементах ионы галлия занимают такое же положение. Этим качественно объясняется наблюдающаяся разница в энергии дефекта упаковки. [34]
Мы исследовали испарение ар-сенида галлия, причем не обнаружили ионов GaAs и обнаружили очень мало ионов галлия. Это объясняется тем, что давление паров галлия гораздо ниже давления паров GaAs, при котором происходит его разложение. [35]
В этом случае п 1, что, учитывая состав комплексов, указывает на замещение ионом галлия в молекуле триоксифлуо-рона одного атома водорода. В двух других случаях либо п 1, что лишено физического смысла, либо экспериментальные значения вообще не укладываются на прямую линию. [36]
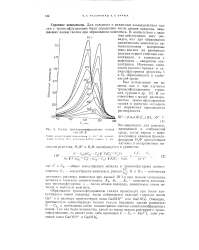 |
Состав трихлорметилфлуороната галлия при рн 8. [37] |
Для суждения о механизме взаимодействия галлия с триоксифлуоронами было определено число атомов водорода, замещаемых ионом галлия при образовании комплекса. В соответствии с законом действующих масс очевидно, что при образовании циклического комплекса с ор-тооксихиноном водородные ионы влияют на равновесие реакции первой степенью концентрации, а комплекса с дифенолом - квадратом концентрации. [38]
В этом случае га 1, что, учитывая состав комплексов, указывает на замещение ионом галлия в молекуле триоксифлуо-рона одного атома водорода. В двух других случаях либо п 1, что лишено физического смысла, либо экспериментальные значения вообще не укладываются на прямую линию. [39]
К исследуемому раствору ( нитрат или перхлорат), содержащему 0 05 - 0 5 ммоля иона галлия, прибавляют точно отмеренный избыток 0 05 М раствора комплексона III, 50 мл 0 1 М боратного буфера и разбавляют до - 100 мл. [40]
 |
Состав трихлорметилфлуороната галлия при рн 8. [41] |
Для суждения о механизме взаимодействия галлия с триоксифлуоронами было определено число атомов водорода, заЦе - щаемых ионом галлия при образовании комплекса. В соответствии с зароком действующих масс очевидно, что при образовании циклического комплекса с ор-тооксихиноном водородные ионы влияют на равновесие реакции первой степенью концентрации, а комплекса с дифенолом - квадратом концентрации. [42]
Кристаллическая структура GaF3 ( InF3) представляет собой плотней-шую упаковку ионов фтора, в октаэдрических пустотах которой расположены ионы галлия. Растворимость GaF3 в воде составляет 2 4 10 - 2 г / л при 25 С, a InF3 - 0 04 г / 100 мл при 22 С. [43]
Все названные азосоединения на основе 8-оксихинолин - 5-сульфокислоты и сульфопроизводных нафтиламина являются хорошими индикаторами для прямого комплексонометрическо-го титрования ионов галлия при рН 2 2 и выше. Однако наиболее селективным индикатором оказалась 7 - ( 4-сульфо - 2-наф-тилазо) - 8-оксихинолин - 5-сулырокислота, позволяющая определять галлий в присутствии достаточно больших количеств ионов щелочноземельных элементов, цинка, кадмия, марганца и алюминия. [44]
Титрование можно проводить и при рН 2 2 - 5 0, причем при высоких значениях рН во избежание гидролиза иона галлия титровать необходимо в присутствии тартрат-ионов. [45]
Страницы: 1 2 3 4