Двухвалентный ион - олово
Cтраница 1
Двухвалентные ионы олова разряжаются без заметной поляризации в результате чего образуются крупные кристаллы олова. [1]
Почему двухвалентный ион олова может проявлять окислительные и восстановительные свойства. [2]
Может ли двухвалентный ион олова проявлять окислитель ные свойства. [3]
Для окисления двухвалентных ионов олова в четырехвалентные в рас-гвор вводят небольшое количество уксуснокислого натрия, а также перекись водорода. [4]
Так как концентрация двухвалентных ионов олова очень мала, то разряд их происходит на предельном токе, что, как правило, приводит к неравномерному беспорядочному росту кристаллов с образованием отдельных мелких конгломератов или микродендритов, скопление которых и составляет губчатую массу. Образование крупных, правильно ограненных кристаллов цинка с преимущественной ориентацией, возможно, связано с концентрационными изменениями в приэлектродном слое во время анодного периода, а также с торможением роста наиболее активных участков ( углов, ступеней или вершин граней) под действием анодной составляющей тока. [5]
Существуют различные способы предупреждения накопления в электролите двухвалентных ионов олова. [6]
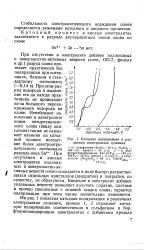 |
Катодная поляризация в различных электролитах лужения. [7] |
Катодный процесс в кислых электролитах заключается в разряде двухвалентных ионов олова. [8]
При недостаточной анодной плотности тока сплав Sn-Zn растворяется с образованием двухвалентных ионов олова, что приводит к выходу электролита из строя. При использовании повышенной анодной плотности тока анод пассивируется, и его растворение протекает с образованием четырехвалентных ионов олова. Выход металлов по току снижается и, если плотность тока была выбрана выше допустимой, пассивная пленка становится такой плотной, что растворение анода прекращается. [9]
Как уже указывалось, щелочные электролиты для лужения не должны содержать двухвалентных ионов олова. [10]
Как уже указывалось, щелочные электролиты для лужения не должны содержать двухвалентных ионов олова. В случае, если в электролите одновременно содержатся двух - и четырехвалентные ионы олова, на катоде в первую очередь будет происходить разряд ионов, в состав которых входит двухвалентное олово, так как разложение станната начинается при значительно более отрицательном потенциале. В результате из таких электролитов олово выделяется в виде губчатых и рыхлых осадков. Если же раствор содержит олово только в четырехвалентной форме, то осаждение металла происходит при высокой катодной поляризации, равной примерно 500 - 600 мв, что, как известно, способствует получению мелкокристаллической структуры. [11]
Наличие стальных анодов вместо оловянных необходимо для регулирования процесса электролиза ( предупреждения образования двухвалентных ионов олова) и требует периодического добавления в электролит солей олова в виде станната натрия. Толщина покрытий колеблется от 10 до 20 мк. По твердости белая бронза уступает хрому, но превосходит никель. [12]
При этом выход по току постепенно снижается примерно до 100 %, что соответствует разряду двухвалентных ионов олова. [13]
Фосфоры, активированные оловом и индием, представляют особый интерес в связи с тем, что двухвалентные ионы олова и одновалентные ионы индия имеют изоэлектронные оболочки, а также ввиду особенностей структуры их спектров поглощения. Исследованные нами фосфоры выращивались в виде монокристаллов либо по методу Киропулоса, либо в откачанных и запаянных кварцевых ампулах. Второй способ выращивания приходится применять в тех случаях, когда активирующая примесь обладает по сравнению с основанием низкой точкой кипения и большой летучестью. [14]
При низких плотностях тока ( до 2 А / дм2) растворение оловянных анодов происходит с образованием двухвалентных ионов олова, а при повышенных ( более 4 А / дм2) - - аноды полностью пассивируются и их растворение прекращается. Растворение оловянных анодов с образованием четырехвалентных ионов олова происходит в интервале 2 - 4 А / дм2; при этом поверхность анодов приобретает желтовато-золотистый оттенок, отвечающий моменту частичной пассивности. [15]
Страницы: 1 2 3