Небольшой ион
Cтраница 1
Небольшие ионы ( например, Li nNa h входят в дырки, имеющиеся в структуре воды. При этом ионы только несколько растягивают и изгибают связи между молекулами воды, не разрывая их. [1]
Небольшие ионы реагируют с белками независимо от суммарного заряда белковой молекулы. Белки способны связывать ( и обычно связывают) катионы и анионы при всех значениях рН, совместимых с сохранением ферментативной активности. Более того, это связывание носит главным образом ионный характер. Объяснение заключается в относительных размерах белков и ионов: маленький ион может видеть одновременно лишь малую часть значительно большей по размеру белковой структуры. Таким образом, ионные взаимодействия ( как и другие виды взаимодействия небольших молекул с белками) строго локализованы на небольших участках поверхности белковой молекулы. Приведенные соображения отнюдь не тривиальны, так как, во-первых, многие субстраты представляют собой небольшие ионы и, во-вторых, ионным взаимодействиям свойственны одновременно и прочность, и обратимость, столь необходимые для образования фермент-субстратного комплекса. [2]
Например, небольшой ион Li входит в полость полиэфира 14-краун - 4, но большие ионы Na и К не помещаются в ней. Стабильность комплекса увеличивается с увеличением числа атомов кислорода, способных к координации, при условии, что они подходящим образом расположены в полиэфирном кольце. [3]
В случае небольших ионов противоположное поляризующее влияние анионов и катионов может промотировать их ассоциацию. [4]
Однако для растворов небольших ионов наблюдаются заметные отклонения от этого правила. [5]
Особенно сильное расщепление вызывают небольшие ионы с высоким зарядом. Благодаря расщеплению орбиталей меняется распределение электронов. Хотя в соответствии с правилом Гунда электроны стремятся занять каждый по орбитали, но под действием такого фактора, как электрический заряд, они все-таки вынуждены спариваться. В таком случае на орбиталях центрального атома освобождаются места для электронов лиганда. Теория кристаллического поля основное внимание уделяет электростатическому взаимодействию центрального иона и лиганда. Она оставляет в стороне изменение свойств лигандов под влиянием центрального атома и не учитывает перекрывание их орбиталей, а ведь фактическая связь в комплексах частично ковалентная. [6]
При диссоциации таких электролитов образуются подвижные небольшие ионы и многозарядный полимерный макроион. [7]
Таким образом, измеряя скорость движения небольших ионов в электрическом поле, обычно определяют величину их подвижности, после чего, используя закон Стокса или связанные с ним уравнения, оценивают их эффективные размеры. Если частицы велики и их общий заряд неизвестен, скорость движения можно связать с - потенциалом. [8]
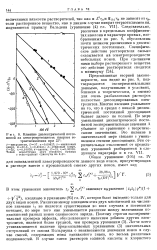 |
Влияние диэлектрической постоянной на электропроводность пикрата те-траэтиламмония при 25. [9] |
Специфическое действие растворителя сильно сказывается на электропроводности небольших ионов. [10]
Диализ, подобно осмосу, представляет миграцию небольших ионов и молекул ( но не коллоидных частиц. В нашем организме такие мембраны играют очень большую роль, так как они разделяют участки тканей, содержащие разные биологические жидкости. [11]
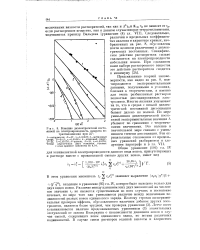 |
Влияние диэлектрической посто. [12] |
Специфическое действие растворителя сильно сказывается на электропроводности небольших ионов. [13]
Это указывает на специфическое взаимодействие катиона с относительно небольшим ионом хлора и на значительное ослабление такого взаимодействия при увеличении размеров иона галогена. [14]
Это обусловлено, вероятно, сильными кулоновскими взаимодействиями небольшого иона Ве2 и прочными водородными связями между плотноупакованными ионами ОН - в Ве ( ОН) 2 ( кр) по сравнению с меньшими ( убывающими при возрастании Z) значениями соответствующих энергий у остальных гидроокисей щелочноземельных металлов. [15]
Страницы: 1 2 3 4