Небольшой ион
Cтраница 4
Каждая молекула ее связана с четырьмя соседними, образуя тетраэдрическую ячейку. Попадая в такую структуру, гростейший небольшой ион благородногазового типа может занять место любой из молекул воды. При этом силами электростатического притяжения или другого вида взаимодействия он плотно свяжется с ближайшим окружением из молекул воды. В простейшем случае при этом наблюдается выделение первичной теплоты растворения. Более сложные ионы могут вовлечь в сферу своего действия и отдаленные слои молекул воды. В этом случае и само взаимодействие усложняется. Выделяемая при этом энергия называется вторичной теплотой гидратации. Крупные ионы ( например, UO b и др.) попадают в теграэдрические пустоты и связываются с большим числом молекул воды. В этом случае благодаря большому размеру иона может произойти значительное нарушение структуры воды и растворенное вещество резко изменит свойства растворителя. [46]
Действительно, известно, что наиболее труднорастворимыми комплексными солями являются те соли, в которых крупный комплексный ион сочетается с крупным же ионом противоположного заряда. Наоборот, при сочетании комплексных ионов с небольшими ионами или, вообще, с такими ионами, при которых установленные выше характерные для минимальных растворимостей отношения rk / ra резко нарушаются, наблюдается очень хорошая растворимость. Известно также, что например, соли аммония ( гни 1 43 А) по своей растворимости проявляют далеко идущую аналогию с солями калия и рубидия. [47]
Решетка состоит из тетраэдров А104 и Si04, имеющих общие углы. В пространствах, образованных этой решеткой, находятся большие ионы хлора и небольшие ионы натрия, показанные на рисунке в виде шаров различных размеров. Минерал лазулит имеет точно такую же структуру с тем отличием, что места ионов хлора занимают полисульфидные группы. [48]
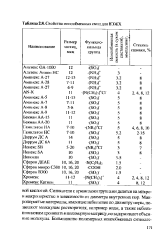 |
Свойства ионообменных смол для ВЭЖХ. [49] |
Силикагели с привитыми группами делятся на микро-и макропористые п зависимости от диаметра внутренних пор. Микропористые материалы, имеющие небольшие по диаметру поры, позволяют молекулам растворителя, например воды, а также небольшим ионам проникать в полимьрную матрицу, но задерживают объемные молекулы. [50]
Предполагая, что ион представляет собой сферическую частицу, можно ( хотя и очень приблизительно) оценить его радиус по подвижности, рассчитанной на основе данных по электропроводности. Разность между значениями радиусов, полученными по кристаллографическим данным и по данным электропроводности ( подвижность ионов), для небольших ионов, например лития, в воде получается очень большой. Это свидетельствует о том, что ион лития окружен очень толстой сольватной оболочкой из молекул воды. [51]
В этих условиях ион окружает прочная соль-ватная оболочка и nhnk. Поскольку согласно уравнению (II.9) электрическое поле иона тем сильнее, чем меньше его радиус, то это характерно для небольших ионов. Так, например, результаты по сжимаемости водных растворов солей лития, по энтропии гидратации и по подвижности иона L1 дают среднее значение л6, соответствующее координационному числу иона лития. [52]
Две другие точки соответствуют растворам в нитрометане и нитробензоле. Эти растворители обладают сравнительно высокой диэлектрической проницаемостью, а сольватация в них слишком слаба, чтобы предотвратить ассоциацию ионов; следовательно, небольшие ионы дают исключительно слабодиссоциирующие соли, причем их растворимости тоже являются низкими. [53]
Чем больше ион, тем меньшей значение имеет сольватация. В то время как трифенилметилхлорид ионизируется только в растворителях, сольвати-рующих ион хлора, трифепилметплнатрий реагирует с растворителями основного характера-эфиром или амином-способными сольватировать небольшой ион натрия и уменьшать концентрацию его заряда. [54]
Степень связывания ионов белками можно определять различными методами; из них наиболее широко распространен метод равновесного диализа. При диализе ( так же как и при осмометрии) используют мешочек, стенки которого непроницаемы для молекул белка, но проницаемы для небольших ионов. Диализный мешочек с раствором белка помещают в раствор, содержащий необходимый ион. После установления равновесной концентрации диффундирующего иона по обе стороны мембраны измеряют концентрацию иона в растворе, не содержащем белка; разность начальной и конечной концентраций иона в не содержащем белка растворе позволяет определить концентрацию иона в растворе белка. Если концентрации иона по обе стороны мембраны равны друг другу, то это означает, что связывания не произошло. Если связывание имело место, то концентрация иона в белковом растворе должна быть выше, чем в растворе, не содержащем белка; разность концентраций может служить мерой числа ионов, связанных с одной молекулой белка. Для того чтобы исключить влияние эффекта Гиббса - Донна-на, равновесный диализ проводят обычно либо в изоэлектрической точке белка, либо при высокой ионной силе. Такие методы, как ультрафильтрация, распределительный анализ, а в некоторых случаях и адсорбционная спектрофотометрия, также могут служить для определения степени связывания ионов с белками. [55]
Цель данной статьи развить и проиллюстрировать, по нашему мнению, обшую, кинетическую модель для реакций второго и более высоких порядков между органическими субстратами и гидрофильными ионами, протекающих в мицеллярных растворах. Эта модель, по существу, представляет собой разумное сочетание кинетических представлений, развитых Березиным и соавторами, и модели Сгиг-тера для распределения небольших ионов. [56]
Страницы: 1 2 3 4