Небольшой ион
Cтраница 3
Как считают некоторые авторы, результаты электрокинетических измерений должны выражаться не через С-потенциал, а через величины, соответствующие тем, которыми пользуются в отношении электролитов, содержащих небольшие ионы, а именно, через подвижности и валентности. Это, однако, связано с тем затруднением, что, несмотря на измерения подвижности, истинные заряды коллоидных частиц или поверхностные плотности их зарядов известны лишь в редких случаях. Заряд и валентность коллоидной частицы должны зависеть от ее размеров, а возможно, и от формы, которые, вероятно, мало влияют на С-потенциал. [31]
Глубокая очистка вещества от ммкропримессй методом электродиализа возможна лишь в гом случае, если мвкроком монет находится в растворе в виде нейтральных молекул, а микрокомпоненты - в виде небольших ионов. Микропримеси Fe3, Al Sn4f, Sb, Bi и другие, образующие при рН 7 малорастворимые гидроокиси, с константой диссоциации меньше 1 10 - 7 обычным методом электродиализа удаляются из растворов в очень небольшой степени. Перенос таких ионов через инертные и электрохимически активные мембраны, как уже отмечалось пыше, крайне затруднен даже при поддержании соотпетстгсующей концентрации ионов водорода и средней камере. Поэтому последнее время применяется введение в среднюю камеру перед электродиализом небольшого количества соответствующего комплексообразующего реагента ( например три-лона Б [13, 18], фторидов щелочных металлов и других), образующего с подобными ионами прочные комплексные ионы, сравнительно легко переносимые через мембраны. [32]
Для соединений типа RA2 - Z характер изменения ДЯ и AZ зависит от размеров иона А: в случае крупных ионов ДЯ и AZ непрерывно уменьшаются, в случае небольших ионов АЯ и AZ непрерывно увеличиваются и, наконец, в промежуточном случае эти функции проходят через минимум. [33]
А, представляющие собой ионы с большим ионным радиусом, вроде Са2, Sr2, Ва2, Cd2, Pb2, La3, Pr3, Nd3, Gd3 или Y3, занимают вершины куба; ион В, являющийся небольшим ионом А13, Сг3, Mn3, Fe3, Ti4 или Мп4, расположен в центре куба. Ионы кислорода расположены в центрах граней. Постоянная решетки составляет около 3 9 А. [34]
Молекулы руг иона и увеличивают его эфзывают гидродинамическим радиуш оны являются источником более сильных электполей, чем большие ионы ( это выводится из электростатической теории, согласно которой электрическое поле на поверхности сферы радиусом К пропорционально ze / R2), и, таким образом, сольватация небольших ионов происходит в большей степени. Небольшие / голы имеют больший гидродинамический радиус, меньшие скорости дрейфа и, следовательно, низкую электропроводность. [35]
Экспериментальные результаты подтверждают первое из этих предположений, но не второе. Небольшие ионы являются источником более сильных электрических полей, чем большие ионы ( это выводится из электростатической теории, согласно которой электрическое поле на поверхности сферы радиусом К пропорционально ze / f ( 2) t и, таким образом, сольватация небольших ионов происходит в большей степени. Небольшие иолы имеют больший гидродинамический радиус, меньшие скорости дрейфа и, следовательно, низкую электропроводность. [36]
Рассмотрим сначала экстракцию растворителями, являющимися представителями алифатических эфиров - диэтиловым и дибутиловым. Поэтому небольшие ионы и ионы умеренного размера, экстрагируемые этими растворителями, будут, за исключением области ничтожно малых концентраций, присутствовать в них главным образом в виде ионных пар. В таком случае член ( А) в числителях уравнений ( 3) и ( 4) будет пренебрежительно малым, а зависимость D от концентрации молибдена будет обусловлена лишь присутствием димера. Точно так же кривая для 4 М НС1 является горизонтальной для Q от 10 - 8 до 10 - 3 М, после чего опять-таки падает. Тот факт, что падение начинается в случае 4 М НС1 при более высокой концентрации молибдена, чем в случае 2 М НС. [37]
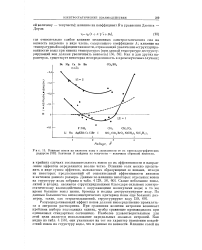 |
Влияние ионов на вязкость воды в зависимости от их кристаллографических радиусов. Значения В найдены из текучести - величины обратной вязкости. [38] |
Самые небольшие ионы, литий и фторид, являются структурирующими благодаря сильному электростатическому взаимодействию с окружающими молекулами воды; в то же время большие ионы цезия, бромида и иодида деструктурируют воду. [39]
В отношении гидратов трудно сделать какие либо обобщения; однако можно указать, что соли больших одновалентных ионов - калия, рубидия, цезия, серебра, золота, таллия и аммония - почти всегда безводны, в то время как многие соли меньших по размерам ионов лития и натрия гидратированы. Многие соли небольшого иона Ве2 гидратированы четырьмя молекулами воды. [40]
Более того, небольшие ионы кремния или алюминия легко могут сместиться из своих положений в тетраэдрах по направлению к центру между тремя оставшимися ионами кислорода, увеличивая электростатическое экранирование, в то время как значительно большие редкоземельные катионы заключены в содалитовых ячейках. Кроме того, отталкивание О-О может иметь большее значение для остова цеолита, чем для иона кислорода, связывающего редкоземельные ионы в содалитовой ячейке. В результате этого больший заряд иона кремния и меньшее расстояние между ионами кремния и алюминия, вероятно, компенсируются другими приведенными здесь факторами и в конечном итоге ион кислорода остается в содалитовой ячейке. [41]
В случае неорганических реакций в твердом состоянии механизм необходимой при этом диффузии через кристаллическую решетку достаточно хорошо изучен. Атомы металлов или небольшие ионы реагирующих веществ перемещаются из своих положений либо в междуузлия решетки, либо в вакансии решетки. Это можно объяснить тем, что такие анионы, как COg -, SO -, РО, слишком велики, чтобы в значительной мере участвовать в процессе диффузии. Следует поэтому ожидать, что в случае органических молекул, более крупных и сложных, чем эти анионы, энергия активации для диффузии в кристаллическом состоянии должна быть весьма высокой. Некоторым доказательством в пользу этого может служить постоянство ( в течение нескольких месяцев) анизотропии спектра электронного парамагнитного резонанса различных органических кристаллов, таких, как глицин [47], аланин [84] и малоновая кислота [79], подвергнутых действию ионизирующей радиации. При измерениях, выполненных с применением меченых атомов на монокристаллах антрацена, было получено значение коэффициента диффузии, равное Ы0 - 10 - 2 - Ю 10 см. сек-1 при 450 К ( на 40 ниже точки плавления) [97], которое на 5 порядков меньше величин, типичных для диффузии в жидкой фазе. Энергия активации для самодиффузии в кристаллах антрацена оценена в 42 ккал / моль. Можно предполагать, что несколько легче диффузия протекает в веществах, находящихся в менее упорядоченном стеклообразном состоянии, которое характерно для органических соединений, способных образовывать водородные связи, но для проверки этой точки зрения никаких данных не имеется. Следует заметить, что при экзотермической реакции в стеклообразном состоянии процесс протекает гораздо легче, так как в точке стеклоподобного перехода скрытая теплота не поглощается. В этой точке подвижность в системе увеличивается в несколько раз. [42]
Несомненно, одним из важнейших факторов, определяющих растворимость, является притяжение между ионами кристалла. Кристаллы, построенные из небольших ионов, которые упакованы более плотно, как правило, сильнее сопротивляются разрушению, чем кристаллы, состоящие из больших ионов. В указанном ряду анионов хлорид-ионы имеют промежуточный размер, и поэтому свойства хлоридов трудно предсказать, основываясь на указанных общих соображениях. [43]
 |
Относительное расположение ионов металлов и молекул воды в гидратах катионов.| Правильный октаэдр. [44] |
Кристаллы двухводного гипса CaSO4 2Н2О обладают слоистой структурой. В плоскости каждого слоя расположены сравнительно небольшие ионы Са2 и крупные ионы SO -, чередуясь примерно в шахматном порядке. Молекулы воды находятся между слоями через два слоя указанных ионов. Каждая из этих молекул связывается с ионом Са2 своим кислородным атомом, а через водородные атомы ( с помощью водородной связи) - с атомами кислорода, содержащимися в ионах SO, принадлежащих противоположному слою. С каждым ионом Са2 связаны по две молекулы воды. [45]
Страницы: 1 2 3 4