Индикаторный ион
Cтраница 1
Индикаторный ион с более низкими электропроводностью и числом переноса должен быть взят соответственно в более низкой концентрации. [1]
Кр системы индикаторный ион / Х известны. [2]
При использовании в качестве индикаторного иона Cd2 может быть определена концентрация следующих лигандов: С1 -, Вг -, J -, NOf, SCN -, NH3, CH3CO2 - - CN - образует прочные комплексы с Cd2, однако восстановление протекает не вполне-обратимо. [3]
Зная константу равновесия образования комплекса индикаторного иона Рь легко найти константу равновесия РГ Здесь, как и выше, важно, чтобы предельный ток первой волны сохранялся по природе диффузионным. [4]
Точность этого метода зависит от устойчивости комплексов индикаторного иона. [5]
Предпосылкой для применения косвенного метода является обратимость восстановления индикаторного иона. Если ион М восстанавливается необратимо, то реакция между М и лиган-дами протекает не мгновенно. В таком случае никогда нельзя1 быть уверенным, что ионы М находятся в равновесии со свободными лигандами у поверхности ртути, хотя концентрации у поверхности электрода могут быть рассчитаны. [6]
Если это осуществляется, то, чем сильнее заряжен индикаторный ион, тем лучше он адсорбируется. Присутствие других сильно заряженных ионов с тем же самым знаком, как у индикаторных ионов, препятствует перенесению индикатора. [7]
Точность косвенного метода зависит от прочности комплексов, образуемых индикаторным ионом. [8]
 |
Кривые потенциометрического титрования. [9] |
Метод Л - титрования основан на использовании электрода, чувствительного к индикаторному иону. При этом индикаторный ион должен находиться в равновесии и с определяемым веществом, и с титрантом, который может образовывать комплексы или малорастворимые соли с этими двумя веществами. Так, например, кальций определяют с помощью медь-селективного электрода: к анализируемому раствору добавляют ионы Си2, а затем титруют раствор ЭДТА. Поскольку титрант образует с Си2 более прочный комплекс, чем с Са2, то на кривой титрования наблюдаются две КТТ: первая соответствует меди, а вторая - кальцию. Если же индикаторный ион образует с титрантом более слабый комплекс, то к анализируемому раствору добавляют избыток титранта и оттитровы-вают непрореагировавший реагент раствором индикаторного иона. Разность между добавленным количеством титранта и его непрореагировавшим количеством позволяет вычислить концентрацию определяемого вещества. В качестве примера можно привести определение фосфат-ионов: к анализируемому раствору добавляют избыток нитрата лантана и оттитровывают непрореагировавшие ионы лантана раствором фторида, используя фторид-селективный электрод. [10]
Если макроколичества соединений носителя и индикатора образуют изоморфные смешанные кристаллы, то индикаторные ионы могут замещать в кристаллической решетке некоторые из ионов вещества носителя одинакового заряда и таким образом переноситься. Эффективность этого процесса переноса зависит от ряда факторов - энергии решетки, образуемой ионами носителя и индикатора в соединении носителя, энергии гидратации ионов индикатора и носителя и применяемого метода осаждения. [11]
РР-К тому же, если ион Ме и восстанавливается на электроде, то индикаторный ион восстанавливается при более положительных потенциалах. [12]
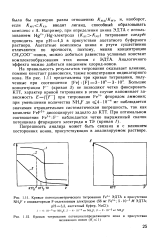 |
Кривые потенциометрического титрования Fe3 ЭДТА в присутствии.| Кривая титрования потенциалопределяющего иона в присутствии. [13] |
На правильность результатов титрования оказывает влияние, помимо констант равновесия, также концентрация индикаторного иона. Большие концентрации F - ( кривая 3) не позволяют четко фиксировать КТТ, характер кривой титрования в этом случае напоминает зависимость Ef [ F - ] при титровании Fe3 фторидом аммония; при уменьшении количества NH4F до 4 - 10 - 4 мг наблюдается значимая отрицательная систематическая погрешность, так как комплекс FeF2 диссоциирует задолго до КТТ. [14]
Даже в том случае, когда ионы носителя и индикатора не являются доста-1 точно сходными для того, чтобы индикаторный ион мог внедриться в решетку соединения носителя, индикатор все же может быть эффективно удален из раствора осадком носителя путем адсорбционного процесса. Теория адсорбции ионов на осадках электролитов рассматривается на стр. [15]
Страницы: 1 2 3