Индикаторный ион
Cтраница 3
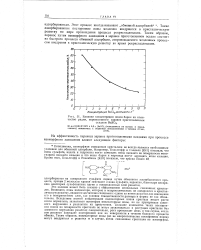 |
Влияние концентрации ионов бария на количество радия, перенесенного заранее приготовленным осадком BaSO j. [31] |
Это явление может быть связано с образованием аномальных смешанных кристаллов. Возможно, ионы индикатора, которые в макроколичествах не внедряются в кристаллическую решетку, являются достаточно сходными с одним из ионов решетки для замещения его в поверхностном слое, где условия тождественности размера и формы не так обязательны. Вследствие низкой концентрации индикаторных ионов кристалл может расти почти нормально, захватывая некоторые индикаторные ионы, но не претерпевая заметного нарушения в результате их присутствия. Большие количества таких посторонних ионов на поверхности кристалла не могут захватываться в растущем кристалле без заметного нарушения решетки; следовательно, рост происходит лишь в том случае, когда ион решетки замещает посторонний ион на поверхности в течение быстрого процесса обмена. Таким образом, индикаторные ионы ( но не макроколичества посторонних ионов) могут внедряться в решетку и в случае, когда смешанные кристаллы не изоморфны. [32]
 |
Электролизер для ам-перометри чес кого титрования. [33] |
Очень важно при амперометрическом титровании знать поведение титруемого вещества или реагента на данном электроде. Если оно неизвестно, то сначала получают кривую сила тока-напряжение каждого из обоих веществ в той же среде, в которой будет проводиться1 титрование. Для одного из них должен получаться хорошо выраженный диффузионный ток, если титрование ведется в отсутствие индикаторного иона. [34]
Оба механизма, Адс1 и Аде 2, начинаются с предравновесного образования сопряженной эфиру кислоты. Поэтому вначале нужно определить кислотную функцию, которая выражает степень этого термодинамически контролируемого переноса протона. Такой наклон, по величине меньший единицы, означает только, что ониевые ионы эфира гидратированы меньше, чем индикаторные ионы Гаммета. [35]
Термин индикатор в этой главе применяется до некоторой степени произвольно; иногда этот термин относится только к радиоактивным атомам, а иногда и к радиоактивным атомам и к изотопным неактивным атомам, которые могут случайно присутствовать. Если термин индикатор употребляется в связи с количеством, измеренным по радиоактивности ( например, измеренное отношение индикатора к носителю, выраженное в отсчетах в 1 мин. Если термин индикатор применяется в связи с химическим термином ( например, концентрация индикатора, вещество индикатора, индикаторный элемент, индикаторное соединение, индикаторный ион), то он относится ко всем изотопным атомам, активным и неактивным. В силу химической идентичности изотопов и та и другая интерпретация может быть использована, когда речь идет о поведении индикатора в реакции. Принимается, что все атомы индикаторного элемента в данной фазе находятся в одинаковой химической форме, за исключением особо оговоренных случаев. [36]
Этот метод основан на измерении скорости движения ионов, определяемой по перемещению границы двух растворов при прохождении тока. В вертикальной трубке имеются два слоя растворов электролитов СА и МА, образующих отчетливую границу, которая при прохождении тока перемещается со скоростью, равной скорости движения ионов. Электролит МА является индикаторным. Для сохранения во время прохождения тока между растворами отчетливой границы прежде всего необходимо, чтобы скорость движения индикаторного иона М была меньше таковой иона С, а плотность верхнего раствора меньше плотности нижнего. [37]
Метод Л - титрования основан на использовании электрода, чувствительного к индикаторному иону. При этом индикаторный ион должен находиться в равновесии и с определяемым веществом, и с титрантом, который может образовывать комплексы или малорастворимые соли с этими двумя веществами. Так, например, кальций определяют с помощью медь-селективного электрода: к анализируемому раствору добавляют ионы Си2, а затем титруют раствор ЭДТА. Поскольку титрант образует с Си2 более прочный комплекс, чем с Са2, то на кривой титрования наблюдаются две КТТ: первая соответствует меди, а вторая - кальцию. Если же индикаторный ион образует с титрантом более слабый комплекс, то к анализируемому раствору добавляют избыток титранта и оттитровы-вают непрореагировавший реагент раствором индикаторного иона. Разность между добавленным количеством титранта и его непрореагировавшим количеством позволяет вычислить концентрацию определяемого вещества. В качестве примера можно привести определение фосфат-ионов: к анализируемому раствору добавляют избыток нитрата лантана и оттитровывают непрореагировавшие ионы лантана раствором фторида, используя фторид-селективный электрод. [38]
Это явление может быть связано с образованием аномальных смешанных кристаллов. Возможно, ионы индикатора, которые в макроколичествах не внедряются в кристаллическую решетку, являются достаточно сходными с одним из ионов решетки для замещения его в поверхностном слое, где условия тождественности размера и формы не так обязательны. Вследствие низкой концентрации индикаторных ионов кристалл может расти почти нормально, захватывая некоторые индикаторные ионы, но не претерпевая заметного нарушения в результате их присутствия. Большие количества таких посторонних ионов на поверхности кристалла не могут захватываться в растущем кристалле без заметного нарушения решетки; следовательно, рост происходит лишь в том случае, когда ион решетки замещает посторонний ион на поверхности в течение быстрого процесса обмена. Таким образом, индикаторные ионы ( но не макроколичества посторонних ионов) могут внедряться в решетку и в случае, когда смешанные кристаллы не изоморфны. [39]
Теорию движения границ разрабатывали Мак-Иннес и Лонгсворт [11], Дол [14], Свенсон [15] и др. для систем, содержащих несколько ионов. Они показали, что в системе с п сортами ионов при одной исходной границе могут образоваться п - 1 границ. При этом в многокомпонентных системах образуются как истинные, так и ложные границы. Истинными обычно называют границы, образованные ведущим и индикаторным ионами, так как только они дают правильное значение подвижности ведущего иона. Ложные границы образованы двумя растворами с разной концентрацией индикаторного иона. Одна из таких границ образуется вблизи первоначального положения и называется е - границей. Образование; ложных границ иногда называют пограничными аномалиями. Это явление затрудняет правильную интерпретацию результатов электрофореза. Пограничные аномалии больше всего проявляются при исследовании веществ с низким молекулярным весом ( большинство неорганических соединений), и поэтому метод фронтального электрофореза широко используют при исследованиях в биологии, преимущественно белков. [40]
При исследовании поведения свободных от носителя индикаторов иногда можно получить некоторые данные, указывающие на состояние окисления индикатора, но такие данные редко являются надежными. Например, изоморфное внедрение индикатора в осадок указывает на то, что заряд, размер и координационное число для ионов носителя и индикатора одинаковы, и это дает возможность определить вероятное состояние окисления индикатора. Например, если не учитывать того факта, что перенос не происходит в щелочных растворах, то можно было бы прийти к выводу, что ионы натрия и свинца сходны, так как хлориды натрия и тория В ( РЬ212) образуют аномальные смешанные кристаллы в кислых и нейтральных растворах ( см. стр. Перенос индикатора путем адсорбции часто дает сведения относительно знака заряда индикаторного иона и растворимости индикаторного соединения. Знание этих свойств полезно для определения степени окисления индикатора. Сведения о летучести индикатора, его растворимости в органических растворителях, скорости диффузии, легкости, с которой он может окисляться и восстанавливаться, и знаке заряда иона индикатора, определяемые при изучении процессов переноса, также следует учитывать при определении степени окисления индикатора. [41]
Метод Л - титрования основан на использовании электрода, чувствительного к индикаторному иону. При этом индикаторный ион должен находиться в равновесии и с определяемым веществом, и с титрантом, который может образовывать комплексы или малорастворимые соли с этими двумя веществами. Так, например, кальций определяют с помощью медь-селективного электрода: к анализируемому раствору добавляют ионы Си2, а затем титруют раствор ЭДТА. Поскольку титрант образует с Си2 более прочный комплекс, чем с Са2, то на кривой титрования наблюдаются две КТТ: первая соответствует меди, а вторая - кальцию. Если же индикаторный ион образует с титрантом более слабый комплекс, то к анализируемому раствору добавляют избыток титранта и оттитровы-вают непрореагировавший реагент раствором индикаторного иона. Разность между добавленным количеством титранта и его непрореагировавшим количеством позволяет вычислить концентрацию определяемого вещества. В качестве примера можно привести определение фосфат-ионов: к анализируемому раствору добавляют избыток нитрата лантана и оттитровывают непрореагировавшие ионы лантана раствором фторида, используя фторид-селективный электрод. [42]
Страницы: 1 2 3