Окрашенный ион
Cтраница 3
Можно также испытуемый раствор, содержащий окрашенные ионы, например хроматы или перманганаты, восстановить, пропуская в подкисленный раствор сероводород. При этом CrOJ переходит в Сг3, а МпО - - в Мп3 и выделяется элементная сера. [31]
При фотолизе лейкоцианида малахитового зеленого образуется окрашенный ион, который стабилен в кислом спиртовом растворе и имеет максимум поглощения при Я 620 нм. Концентрация раствора выбирается таким образом, чтобы поглощение его в кювете на актинометрируемой длине волны было полным. Определенный объем V актинометра помещают в кювету и подвергают фотолизу в течение различных промежутков времени. Время облучения выбирается так, чтобы оптическая плотность при Я 620 нм не превышала 0 15, поскольку образующиеся ионы поглощают ультрафиолетовый свет и могут действовать как внутренний фильтр. Это приводит к заниженным результатам. После облучения измеряют оптическую плотность при Х 620 нм и строят график ее зависимости от времени фотолиза. [32]
 |
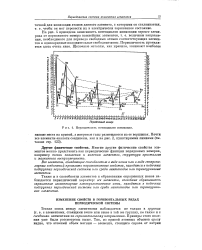
Максимумы поглощения растворов красителей. [33] |
На чем основано колориметрическое определение концентрации окрашенных ионов. [34]
Если определяют следы хрома и концентрации посторонних окрашенных ионов не слишком велики, то холостой опыт можно провести после измерения оптической плотности анализируемого раствора, восстановив в нем хромат добавлением соли Мора. [35]
В зависимости от кислотности или щелочности раствора окрашенный ион красителя может оказаться или анионом или катионом. Так, например, флуоресцеин в кислой среде является цоложительным ионом, а в щелочной - теряет три протона и становится двухвалентным анионом. [36]
 |
Периодичность потенциалов ионизации. [37] |
Также и в способности элементов к образованию окрашенных ионов наблюдается периодический характер: все элементы, способные образовывать окрашенные элементарные электролитические ионы, находятся в побочных подгруппах периодической системы или среди лантанидов или трансурановых элементов. [38]
При наличии в растворе сильнопротолизующихся солей и окрашенных ионов нужно удалить мешающие ионы. [39]
Также и в способности элементов к образованию окрашенных ионов наблюдается периодический характер: все элементы, способные образовывать окрашенные элементарные электролитические ионы, находятся в побочных подгруппах периодической системы или среди лантанидов или трансуранов. [40]
Также и в способности элементов к образованию окрашенных ионов наблюдается периодический характер: все элементы, способные образовывать окрашенные элементарные электролитические ионы, находятся в побочных подгруппах периодической системы или среди лантанидов или трансу ранов. [41]
Как уже отмечалось, образование комплексных соединений окрашенных ионов сопровождается обычно углублением окраски, которую легко измерить фотометрически. Это свойство было использовано Суитсером и Бриккером [25] для определения меди и никеля. Таким же способом Ундервуд [33] определяет железо и медь при их совместном присутствии. [42]
Предложенная схема отличается от обычной схемы образования окрашенного иона XXIV в щелочном растворе ( XXI - XXV - XXIV) тем, что здесь за первую стадию реакции принимается атака основания на одну из феноль-ных гидроксильных групп, а не на лактонное кольцо. Образующееся соединение XXIV представляет собой хиноидную структуру, стабилизированную ионом карбоксила благодаря электронному сдвигу, показанному на схеме. [43]
Страницы: 1 2 3