Благородный газ
Cтраница 1
Благородный газ является тем перевалочным пунктом, который отделяет типичный неметалл данного периода от типичного металла, открывающего следующий период. В первом периоде, кроме гелия, имеется только один элемент - водороду значит, следует ожидать, что водород сочетает свойства, типичные как для металлов, так и для неметаллов. [1]
 |
Схематическое изображение периодической системы элементов Д. И. Менделеева. [2] |
Благородный газ является элементом, отделяющим типичный неметалл данного периода от типичного металла, открывающего следующий период. В первом периоде кроме гелия имеется только один элемент - водород; значит, следует ожидать, что водород сочетает свойства, типичные как для металлов, так и для неметаллов. [3]
Использование благородных газов в больших масштабах связано главным образом с их высокой инертностью. Около 30 % гелия используют в космической технике для вытеснения жидкого кислорода и водорода в ракетах. Примерно 20 % его расходуется на атомных электростанциях в качестве теплоносителя, так как гелий не вступает в химические и ядерные реакции и характеризуется высокой теплопроводностью, низкой вязкостью и плотностью. Около 18 % гелия используют при дуговой сварке в атмосфере инертного газа, 12 % в метеорологических зондах и остальное - при необходимости создания искусственной атмосферы для дыхания. Низкие вязкость и молекулярный вес гелия облегчают дыхание и дают возможность рабочему не перегреваться, что позволяет значительно повысить производительность труда. Это позволяет сократить период декомпрессии и уменьшить его опасность для организма человека. [4]
 |
Некоторые ионы, изоэлектронные с атомами благородных газов. [5] |
Поведение благородных газов очень близко к поведению идеального газа в широком диапазоне изменения условий. [6]
Кроме благородных газов, существует только одна группа элементов, которые находятся в газообразном состоянии в обычных лабораторных условиях - это элементы группы галогенов. Мы не будем рассматривать здесь астат, так как он не имеет устойчивых изотопов. Данные о реагирующих объемах, расчеты по методу Канниццаро, данные о теплоемкостях и многие другие факты свидетельствуют о том, что при обычных условиях элементы фтор, хлор, бром и иод представляют собой газы, состоящие из двухатомных молекул F2, C12, Вг2, Ь - В жидком и твердом состояниях эти элементы также состоят из двухатомных молекул. При высоких температурах двухатомные молекулы газообразных галогенов диссоциируют на атомы. Степень диссоциации при одинаковой температуре Т уменьшается от иода к брому и хлору, однако фтор диссоциирует почти так же, как и иод. [7]
Кристаллы благородных газов также молекулярные, построены из одноатомных молекул. Первые состоят из одинаковых молекул, вторые-из разных. [8]
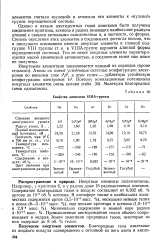 |
Свойства элементов VIHA-группы. [9] |
Молекулы благородных газов одноатомны. [10]
Конфигурации благородных газов давно считались устойчивыми. Помимо того, что это правило Сиджвика неудачно, так как имеет дело с различными числами электронов для разных благородных газов, оно еще и часто не выполняется - соединения имеют другую стехиометрию. Правило 18 электронов очень часто используют для предсказания состава различных металлорганических соединений, особенно карбонильных и нитрозильных. [11]
Клатраты благородных газов с гидрохиноном приобрели практическое значение как наиболее устойчивые из всех молекулярных соединений с неспецифическими силами взаимодействия, открытых до настоящего времени. Устойчивость клатратов благородных газов с гидрохиноном повышается от аргона к ксенону. Клатрат криптона вполне устойчив при комнатной температуре. Они предложили применять гидрохиноновый клатрат 85Кт в качестве 3-источника. [12]
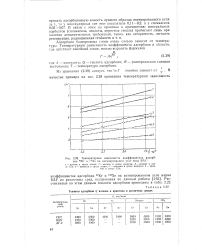 |
Температурная зависимость коэффициентов адсорбции 85Кг и 133Хе на активированном угле типа БАУ.| Теплоты адсорбции Q ксенона и криптона в различных средах. [13] |
Адсорбция благородных газов очень сильно зависит от температуры. [14]
Химия благородных газов интенсивно изучается, намечаются пути практического использования результатов исследований. Делаются попытки улавливать в виде фторидов выделяющиеся в атомных реакторах радиоактивные криптон и ксенон. Фториды используются в качестве фторирующих и окисляющих агентов. Оксиды ксенона представляют интерес как взрывчатые вещества, не оставляющие при взрыве твердых остатков. [15]
Страницы: 1 2 3 4