Благородный газ
Cтраница 2
Атомы благородных газов обладают слабой реакционной способностью. [16]
 |
Изменение радиусов атомов с увеличением атомного веса. [17] |
У благородных газов увеличивается и энергия ионизации по сравнению с предшествующими элементами данных периодов. [18]
Химия благородных газов интенсивно изучается, намечаются пути практического использования результатов исследований. Делаются попытки улавливать в виде фторидов выделяющиеся в атомных реакторах радиоактивные криптон и ксенон. Фториды используются в качестве фторирующих и окисляющих агентов. Оксиды ксенона представляют интерес как взрывчатые вещества, не оставляющие при взрыве твердых остатков. [19]
КлаЬки благородных газов очень невелики: от 10 % у аргона до 10 для радона. Таким образом, и в VIIIA-группе действует общее геохимическое правило - наиболее распространенным является элемент третьего периода периодической системы. [20]
Из благородных газов наибольшую опасность для человека представляют радиоактивный радон и радиоактивные изотопы ксенона, образующиеся при работе атомных электростанций и на урановых рудниках. [21]
Вдыхание благородных газов, особенно Кг и Хе, под давлением вызывает наркотическое действие. В частности, пребывание в атмосфере, содержащей 70 % Хе и кислород, приводит к потере сознания через 2 - 4 мин. Вдыхание гелиево-кислородной смеси позволяет водолазам спускаться на большие глубины, чем при вдыхании воздуха. [22]
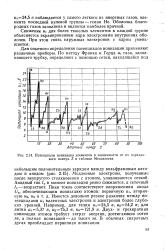 |
Потенциалы ионизации элементов в зависимости от их порядкового номера Z в таблице Менделеева. [23] |
Оболочка благородных газов заполнена и является наиболее прочной. [24]
Соединения благородных газов и бэра обычно довольно подроб-о рассматривают в книгах по общей неорганической химии, их структура, описанная в гл. [25]
Теплоемкость благородных газов и паров металлов равна 3R / 2 и не зависит от температуры. Лишь в случае гелия обнаружено уменьшение теплоемкости при очень низких температурах. [26]
Применение благородных газов в различных областях науки и техники все возрастает. [27]
Присутствие благородных газов в воздухе было постулировано ( а затем открыто) У. Плотность какого азота должна быть больше. [28]
Соединения благородных газов и бэра обычно довольно подроб-о рассматривают в книгах по общей неорганической химии, их структура, описанная в гл. [29]
Атомы благородных газов можно представить себе соединенными ван-дер-ваальсовыми силами не только с другими атомами благородных газов или близкими к ним по свойствам молекулам, но и с молекулами, которые сильно от них отличаются. Тогда в кристаллической решетке такого соединения соотношение между числом атомов благородного газа и числом молекул второго вещества должно быть постоянным, так как на место атома благородного газа нельзя поставить не сходную с ним молекулу второго вещества. Мы будем иметь в этом случае химическое соединение постоянного состава с определенной химической формулой, и чем больше ван-дер-ваальсовы силы у компонента, соединяющегося с благородным газом, тем устойчивее будет соединение. Такое соединение может иметь температуру плавления гораздо более высокую, чем кристаллы благородного газа. Действительно, известно несколько соединений благородных газов, которые следует отнести к этому классу веществ: это гидраты аргона, криптона и ксенона. Повидимому, молекулярные кристаллогидраты представляют собой одну из наиболее устойчивых групп молекулярных соединений, насчитывающих несколько десятков представителей. Эта группа молекулярных соединений изучена сравнительно лучше, чем другие молекулярные соединения. [30]
Страницы: 1 2 3 4