Благородный газ
Cтраница 3
Разделение благородных газов методом изоморфного соосаждения с гидратом двуокиси серы не имеет никаких преимуществ перед разделением чисто физическими методами и было предпринято лишь для того, чтобы окончательно разбить старый предрассудок о полной химической инертности благородных газов. Здесь очень наглядно можно показать разницу в химических свойствах отдельных благородных газов и отчетливо увидеть, с какой легкостью благородные газы образуют химические соединения. Действительно, отделить радон от неона и гелия можно всего лишь за 10 минут и это сделать гораздо проще, чем отделить цезий от натрия. [31]
Разделение благородных газов было предпринято также и для того, чтобы показать, что молекулярные соединения можно не только изучать, но и производить с ними определенные химические операции. Наконец, оно было предпринято для того, чтобы экспериментально обосновать новый метод количественного осаждения газового компонента твердых диссоциирующих соединений. Этот метод может найти очень широкое применение в различных областях химии. [32]
У благородных газов Е равно нулю. При присоединении двух электронов к атомам О и S не выделяется, а поглощается 7 3 и 3 4 эв энергии соответственно. Интересно, что у фтора сродство к электрону меньше, чем у хлора. [33]
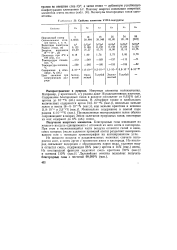 |
Свойства элементов VIIIA-подгруппы. [34] |
Молекулы благородных газов одноатомны. [35]
 |
Теплоемкость и число степеней свободы. [36] |
Теплоемкость благородных газов и паров металлов равна 3 R / 2 и не зависит от температуры. Лишь в случае гелия обнаружено уменьшение теплоемкости при очень низких температурах. Если г 2, то теплоемкость в противоречие с табл. XI 1.1 увеличивается при повышении температуры. При этом данные седьмого столбца правильно передают лишь асимптотическое значение теплоемкости при высоких температурах. [37]
У благородных газов Е равно нулю. При присоединении двух электронов к атомам О и S не выделяется, а поглощается 7 3 и 3 4 эВ энергии соответственно. Интересно, что у фтора сродство к электрону меньше, чем у хлора. [38]
Атомы благородных газов ( Не, Ne, Аг, Кг, Хе, Rn) занимают в таблице особое положение - в каждом из них заканчивается заполнение перечисленных в ( 73 1) групп состояний. С этим связана и химическая инертность этих элементов. [39]
 |
Потенциалы ионизации элементов в зависимости от их порядкового номера 2 в таблице Менделеева. [40] |
Оболочка благородных газов заполнена и поэтому наиболее прочна. [41]
Конфигурация благородного газа у аргона получается потому, что состояние Зр, с одной стороны, и состояния 3d и 4s, с другой стороны, сильно разнятся энергетически. Можно сказать, что у аргона сравниваются влияния главного и азимутального квантовых чисел на энергию уровня: они влияют примерно одинаково и еще достаточно сильно, чтобы этот элемент имел устойчивую электронную оболочку благородного газа. Но в отличие от гелия аргон все же способен вступать в химические соединения. [42]
Атомы благородных газов ( Не, Ne, Ar, Kr, Xe, Rn) занимают в таблице особое положение - в каждом из них заканчивается заполнение перечисленных в (73.1) групп состояний. С этим связана и химическая инертность этих элементов. [43]
Атомы благородных газов, например Rn, могут изоморфно замещать молекулы SO2, CO2, СНзСОСН3 и др. По этому способу образуются все истинные смешанные кристаллы. [44]
Способность благородных газов к образованию соединений не ограничивается приведенными выше примерами. Получены также соединения радона с толуолом, и число подобных молекулярных соединений в будущем еще несомненно умножится. Сам факт существования комплексов благородных газов позволяет применять к ним в ряде случаев обычные методы химических исследований, что прежде казалось невозможным. [45]
Страницы: 1 2 3 4