Свободный ион - металл
Cтраница 1
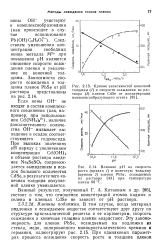
Свободные ионы металлов быстро удаляются из крови; по данным Д. И. Семенова и И. П. Трегубенко ( 1958), - в течение 5 минут. Они также быстро выделяются из организма или накапливаются в скелете. Последнее, так же как и быстрое выделение с мочой, обычно указывает на то, что металл в организме циркулирует в ионизированном или молекулярно-дисперсном состоянии. [1]
Известна концентрация свободных ионов металла и, следовательно, также свободных лигандов. [2]
Измеряется концентрация свободных ионов металла. [3]
Более низким концентрациям свободных ионов металла соответствуют точки в нижней части рисунка. [4]
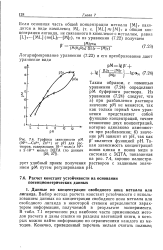 |
Графики зависимости рМ ( М2 - Си2, Zn2 от рН для растворов, содержащих 10 - 3 моль / л М2 а 2 - Ю-3 моль / л ЭДТА ( по данным. [5] |
Данные по концентрации свободного иона металла или лиганда. Выбор метода расчета констант устойчивости с использованием данных по концентрации свободного иона металла или свободного лиганда в некоторой степени определяется характером информации, получаемой в результате эксперимента. В табл. 7.1 перечислен ряд наиболее часто применяемых методов расчета и даны ссылки на разделы настоящей книги, в которых можно найти информацию по ограничениям каждого из методов. [6]
Следовательно, концентрация свободного иона металла М убывает по мере увеличения значения PMY и уменьшения исходной концентрации металла. [7]
Следствием уменьшения концентрации свободных ионов металла М2 при повышении рН являются снижение скорости осаждения пленки и увеличение ее конечной толщины. [9]
Разумеется, на самом деле свободные ионы металла являются в той или иной степени гидратированными. [10]
Разумеется, на самом деле свободные ионы металла являются в той или иной степени гпдратированными. [11]
При реакциях комплексообразования концентрация свободных ионов металла снижается вследствие образования комплексного соединения. Уменьшение концентрации ионов комплексообразователя зависит от константы неустойчивости образующегося комплекса и концентрации комплексующего вещества. [12]
МА ] - концентрация свободных ионов металла, образующихся при диссоциации комплекса, который является продуктом реакции маскирования. [13]
Стало быть, концентрация свободного иона металла в этой области рН пропорциональна третьей степени концентрации ионов водорода. [14]
В тех случаях, когда свободный ион металла не вступает в реакцию обмена с облучаемым соединением и разделение этих форм возможно, для разделения по методу Сцилларда - Чалмерса удобно проводить облучения металлоорганических соединений и комплексных солей. Хорошие результаты были получены при облучении какодиловой кислоты ( CH3) 2AsOOH, из которой As76 выделяется в виде арсенита серебра с 95 % - ным выходом; медной соли о-фенилендиаминсалицилового альдегида, из которой можно выделить почти 97 % радиоактивной меди в виде иона Си2; уранилбензоилацетоната U02 ( CeH5COCHCOCH3) 2, из которого радиоактивный U239 был извлечен с почти 10 % - ным выходом. [15]
Страницы: 1 2 3 4