Простой ион
Cтраница 2
Способность простых ионов образовывать такие комплексные соединения, особенно в концентрированных растворах, проявляется весьма часто. Простые ионы могут присоединять нейтральные молекулы и. Если простой ион Присоединяет к себе нейтральную молекулу, например НзО, НЮа, NHs, или органические ( молекулы, то не происходит никакого изменения ни в первоначальной валентности, ни в электрическом заряде. [16]
Наличие простых ионов Bi доказано только для растворов перхлората висмута, содержащих много свободной кислоты. [17]
 |
Катодная поляризация выделение металлов из цианидных в цинковых сульфатных и циа - электролитов происходит в результате. [18] |
Под простыми ионами здесь и далее подразумеваются аквакомплексы. [19]
В простых ионах обычно заряд его, а также степень окисления и валентность элемента совпадают. В сложных ионах это не обязательно. [20]
Обнаружить поэтому простые ионы Fe2, Fe3, CN, Pt4 в растворах их комплексных солей применяемыми в аналитической химии реактивами не удается. [21]
Вещества, содержащие простые ионы Hg, называются окисями. [22]
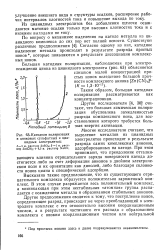
Собственная флуоресценция простых ионов характерна для растворов уранила и некоторых элементов группы редких земель; она отмечена также при описании флуоресцентных определений этих элементов. Описанное явление практического применения в анализе еще не имеет. [23]
Иногда маскировка простых ионов происходит помимо желания аналитика, за счет образования еще не изученных комплексных соединений. [24]
Потенциал полуволны простого иона метал а определен для азотнокислых солей. [25]
В случае простых ионов равновесие наступает, когда по обеим сторонам мембраны имеется одинаковый электрохимический потенциал. Однако неравномерное распределение ионов, обусловленное доннановским эффектом, создает и при равновесии разность концентраций, что должно приводить и к разности электрических потенциалов. [26]
Небольшие количества простых ионов и ионных тройников обусловливают ряд заметных кинетических эффектов. Однако выше концентрации 10 - 2 М, когда преобладают высшие агрегаты, трудно ожидать, что реакция с солями будет подчиняться простым кинетическим закономерностям. [27]
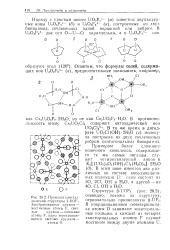 |
Проекция кристаллической структуры P - UOF4, Заштрихованные кружки - мостиковые атомы F, светлые кружки - концевые атомы F, пары перекрывающихся светлых кружков - атомы О. [28] |
Наряду с простым ионом U02F53 - ( а) известны двухъядер-иые ионы U2O4F95 - ( б) и U2O4F84 - ( в), построенные из двух бипирамнд, сочлененных одной вершиной пли ребром. [29]
При присоединении простыми ионами ионов противоположного заряда происходит изменение первоначальной зарядности простых ионов. [30]
Страницы: 1 2 3 4