Простой ион
Cтраница 3
Известно, что простые ионы не мешают определению. Такие ионы, как сульфит, нитрит и пероксиды, сразу окисляются избытком Мпш. [31]
Способность элементов образовывать простые ионы обусловлена электронной структурой их атомов. [32]
В водных растворах простые ионы большинства металлов ( кроме щелочных) устойчивы только в кислых растворах. [33]
Скетчарда, сумма простых ионов, включенных в компонент, равна 0 и vh в уравнении ( 20 - 7) может быть взято с учетом только объема макроиона. Для макроионов небольшого заряда, например для белков вблизи их изоэлектрических точек, это будет правильным независимо от того, как определяются компоненты, так как объем небольшого числа неорганических ионов пренебрежимо мал по сравнению с объемом частиц макроиона. Ниже, как правило, используется уравнение ( 20 - 6) для объема гидродинамических частиц, образованных макроионами в сильно разбавленных растворах солей. При этом имеются в виду упомянутые выше допущения. [34]
Определение потенциала полуволны простого иона производят в присутствии фона, который не образует комплексных соединений с исследуемым ионом, как например нитрат или хлорат калия. [35]
Химические связи между комплексными и простыми ионами в процессе электролитической диссоциации сравнительно легко раскрываются и подчиняются известным правилам о валентности. Связи, приводящие к образованию комплексных ионов, получили название донорно-акцепторных связей. [36]
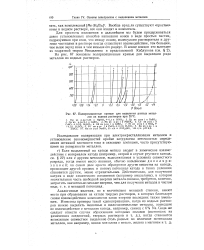 |
Поляризационные кривые для выделения разных металлов из водных растворов при 209С. [37] |
Вообще вряд ли существуют простые ионы в водном растворе, все они входят в комплексы. [38]
 |
Константы неустойчивое некоторых комплексных ионов. [39] |
Этим объясняется, что простые ионы, входящие в состав комплексного иона, удается открыть одними реактивами, а другими, менее чувствительными, открыть не: удается. [40]
Однако в таком состоянии простых ионов они не образуют. По сравнению с VA-подгруппой усиливается их комплексообразующая способность. Окислительно-восстановительный потенциал элементов подгруппы кислорода положительнее водорода и уменьшается от кислорода к полонию. Поэтому Se, Те и Ро не вытесняют водород из растворов и получают их электролизом водных растворов соединений, содержащих простые ионы. С водородом они образуют соединения с полярной ковалентной связью со смещением электронных пар от водорода к элементу. Однако уже соединение Ir Te является неустойчивым эндотермическим соединением. У полония и в меньшей степени у теллура про являются свойства образовывать катионы. [41]
Возникающее таким путем окрашивание простых ионов или комплексов, содержащих некоторые металлы, например, окрашивание желтого иона СгО -, или пурпурного МпО -, или кобальт-аммиакатов, характеризующихся яркими цветами, изменяющимися от одного конца спектра до другого, не относится к рассматриваемому вопросу. [42]
Он состоит как из простых ионов: анионов кислорода и серы ( О2 -, S2 -), катионов кальция, магния, железа ( Са2, Mg2, Fe2, Fe3), так и сложных анионов - главным образом силикатных. Образование сложных силикатных анионов объясняется очень сильным взаимодействием между атомами кремния и кислорода, которое возникает вследствие того, что четырехзарядный ион кремния Si4 с таким большим зарядом отличается малым геометрическим размером. Поэтому электрическое поле вокруг такой частицы очень велико и, как видно из уравнения ( VII-1), она должна очень сильно притягивать к себе противоположно заряженные ионы кислорода. [43]
Наличие резкого перехода от простых ионов к мицеллам очень хорошо подтверждается изменением характера зависимости эквивалентной электропроводности от концентрации. Эти изломы являются очень резкими в случае солянокислых октадециламина и гексадециламина и делаются более плавными по мере уменьшения числа атомов углерода в катионе. Кривая для соля-локислого октиламина уже является типичной для нормального сильного 1 1-электролита. [44]
Обменные реакции с участием простых ионов идут с большой скоростью, лимитируемой практически только скоростью поступления исходных веществ в зону реакции. Поэтому при простом слиянии, а тем более перемешивании двух концентрированных растворов ( пусть тех же СаС12 и KF), почти мгновенно проходящая реакция образования CaF2 приводит к образованию раствора этого вещества, по концентрации в сотни раз большей, чем концентрация насыщения. Вообще, малорастворимые соединения имеют очень большую ширину метастабильной зоны. Если же раствор достигает лабильной области, то происходит множественное зародыше-образование, приводящее к появлению мелкокристаллического, а то и коллоидного материала. Предотвратить это можно, либо существенно замедлив поступление исходных веществ в зону реакции, либо использовав растворы пониженной концентрации. Второй вариант более прост, поэтому начнем с него. Для целого ряда физических исследований достаточно иметь кристаллы с размерами, не превышающими десятые и сотые доли миллиметра. Для получения таких кристаллов [ Мошкин С. В. и др., 1980 ] требуется всего лишь чашка Петри с крышкой и пара стеклянных полосок толщиной 1 - 1 5 мм. Растворы сливаются в колбу, которая встряхивается 5 - 10 с, после чего раствор выливается в большую емкость чашки Петри ( крышку) с положенными в нее заранее упомянутыми полосками стекла. Затем меньшая емкость, донной частью вниз, вводится внутрь большой и ставится на стеклянные полоски. Кристаллизация идет в растворе, находящемся в узкой щели между донными частями емкостей. Возникающие кристаллы способствуют быстрому снижению пересыщения и прекращению зародышеобразования. Отсутствие контакта раствора с воздухом также уменьшает вероятность возникновения зародышей сверх тех, которые возникли при смешении. Через несколько часов кристаллизация заканчивается, крышка вынимается, раствор осторожно сливается, а его остатки оттягиваются фильтровальной бумагой. Без извлечения кристаллов этот метод успешно используется для изучения под микроскопом особенностей кристаллизации, в частности, гипса. [45]
Страницы: 1 2 3 4