Поливалентный ион
Cтраница 3
С электрохимической точки зрения всякий ионнт представляет собой нерастворимый сложный поливалентный ион, связанный ионной связью с подвижными ионами противоположного знака. [31]
Специфичность поглощения ионов определяется зарядом ( для поливалентных ионов специфичность значительно выше, чем для одновалентных), размерами иона в гидратированном состоянии и другими факторами, в том числе свойствами органической основы, матрицы ионита ( см. разд. Некоторые смолы проявляют склонность к образованию дополнительных, комплексных связей с ионами, такие смолы называют хелатньми. [32]
По своей структуре всякий ионит состоит из нерастворимых поливалентных ионов, несущих положительный или отрицательный заряд и окруженных подвижными ионами противоположного знака. [33]
Добавка карбоната натрия в жидкость затворения, содержащую поливалентные ионы ( Са2, Mg2 и др.), может привести к резкому снижению прокачиваемости тампонажного раствора из-за образования дополнительной твердой фазы в виде карбоната кальция и др. При добавке акриловых полимеров совместно с хромпиком в шлаковые тампонажные растворы, термостойкость последних составляет около 200 С. При этом если полимер в чистом виде подвергается термоокислительной деструкции, например, при 250 С, то как замедлитель схватывания может применяться только до 120 С, что связано с десорбцией реагента с зерен цемента и переход его в раствор. Поэтому при использовании регуляторов свойств тампонажных растворов необходимо, чтобы предельная температура их применения была на 30 - 40 С ниже температуры термоокислительной деструкции реагента. [34]
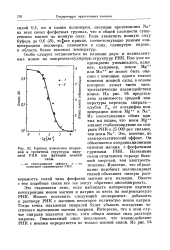 |
Кривая изменения вторич - связями магния с фосфатными. [35] |
Особо следует остановиться на влиянии двух - и поливалентных ионов на макромолекулярную структуру РНК. Как уже неоднократно упоминалось, влияние, например, ионов Mg или Мп не может быть описано с помощью одного только понятия ионной силы, в основе которого лежат чисто электростатические взаимодействия ионов. Это, конечно, не электростатический эффект. [36]
Этот эффект приводит к снижению энергий электростатического взаимодействия поливалентного иона с ионитом. Естественно, что он, отсутствует в случае адсорбции одновалентного иона. [37]
Согласно правилу Шульце - Гарди, при коагуляции золей поливалентными ионами порог коагуляции уменьшается: коагулирующая способность двухвалентных ионов приблизительно в 50 раз, а трехвалентных в 1000 раз больше, чем одновалентных. [38]
Для коагуляции золя смесями электролитов часто требуется большее количество поливалентного иона, чем в отсутствии второго электролита. Это явление повышения порога коагуляции в смеси электролитов называется антагонизмом ионов; оно обычно наблюдается для разновалент-ных ионов, например, для ионов А13 и К при коагуляции золя AgJ. [39]
Для коагуляции золя смесями электролитов часто требуется большее количество поливалентного иона, чем в отсутствие второго электролита. Это явление повышения порога коагуляции в смеси электролитов называется антагонизмом ионов; оно обычно наблюдается для разновалентных ионов, например для ионов А13 и К при коагуляции золя Agl. В некоторых случаях при коагуляции смесями электролитов наблюдается понижение порогов коагуляции - синергизм ионов. [40]
Такое явление связано с процессом замещения обменных ионов минерала на поливалентные ионы раствора, усиливающимся по мере роста температуры и концентрации последнего. [41]
Таким образом, с электрохимической точки зрения всякий ионит представляет собой нерастворимый сложный поливалентный ион, который связан ионной связью с подвижными ионами с зарядом противоположного знака. [42]
 |
Чередование зон устойчивости. [43] |
Чередование зон устойчивости характерно для электролитов, коагулирующие ионы которых - поливалентные ионы Fe8, Тп4 Сг3 и органические ионы. Как видно на рисунке, уменьшение абсолютной величины заряда частицы совпадает с первой областью коагуляции. [44]
С применением карбоксильных катионитов типа КБ-4, КБ-2, селективно поглощающих поливалентные ионы, стало возможным извлекать Ni21, Со2, Сг34 и др. из растворов смесей электролитов. Указанные катионы хорошо сорбируются из растворов, содержащих большое количество солей щелочных металлов на Na-катионите карбоксильного типа. Этот процесс имеет большое значение для гидрометаллургии. [45]
Страницы: 1 2 3 4