Вводимый ион
Cтраница 2
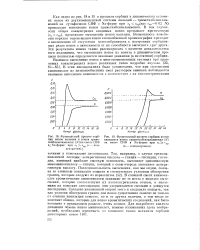
Увеличение концентрации вводимого иона вызывает обострение фронта ( границы) зон, если ион с меньшей валентностью вытесняет ион с большей валентностью. Уменьшение концентрации вводимого иона, наоборот, вызывает обострение фронта при вытеснении иона с меньшей валентностью или приводит к размыванию фронта при вытеснении иона с большей валентностью. [16]
Как видно из рис. 18 и 19 в процессе сорбции в динамических условиях ионов из двухкомпонентной системы кальций - триметилбензилам-моний на сульфосмоле СНФ в Na-форме при с с р ( где скр 0 02 N) происходит вытеснение ионов триметилбензиламмония. В том случае, если общая концентрация вводимых ионов превышает критическую ( с0 скр), происходит вытеснение ионов кальция. Возможность изменения порядка перемещения ионов в ионообменной хроматографии приводит к заключению об отсутствии целесообразности в построении сорбцион-ных рядов ионов в зависимости от их способности вытеснять друг друга. Эти результаты можно также рассматривать в качестве доказательства того положения, что вытеснение ионов из ионита в динамическом процессе полностью определяется законами динамики ( а не статики) сорбции. [18]
Поэтому электропроводность слоев, полученных ионным легированием, существенно отличается - от электропроводности, вычисленной исходя из концентрации введенных примесных атомов. Степень отличия этих двух величин называется коэффициентом использования вводимых ионов. [19]
Данные опыта свидетельствуют о том, что максимальная концентрация ингибирующих добавок, при которых промывочные жидкости чувствительны по изменению электрического сопротивления к действию солей и химических реагентов различна для каждой из исследуемых солей. Этот эффект связан с тем, что увеличение количества вводимых ионов до определенной концентрации увеличивает электропроводность промывочных жидкостей, когда разрушающее действие на структуру воды увеличивает подвижность молекул. При увеличении концентрации солей рост электропроводности становится менее интенсивным, что связано с уменьшением подвижности ионов. [20]
Эффект влияния вводимых ионов в существенной степени определяется энергией гидратации ионов. Установлена четкая закономерность - с повышением энтальпии гидратации ионов растет эффект действия вводимых ионов. [21]
 |
Типичные кривые потенциометрического титрования. [22] |
При потенциометриче-ском титровании к индикаторным электродам не предъявляются такие строгие требования. В этом случае электроды должны обеспечивать закономерное изменение потенциала с концентрацией определяемых или вводимых ионов. [23]
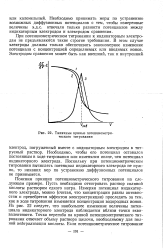 |
Типичные кривые потенциометри-ческого титрования. [24] |
При потенциометрическом титровании к индикаторным электродам не предъявляются такие строгие требования. В этом случае электроды должны только обеспечивать закономерное изменение потенциала с концентрацией определяемых или вводимых ионов. [25]
Таким образом, растворимость электролита уменьшается от введения в раствор одноименных ионов. Исключением являются те случаи, когда происходит связывание одного из находящихся в растворе ионов с вводимыми ионами в более сложные ( комплексные) ионы ( см. гл. [26]
Таким образом, растворимость электролита уменьшается от ведения в раствор одноименных ионов. Исключением являются те лучаи, когда происходит связывание одного из находящихся в створе ионов с вводимыми ионами в более сложные ( комплекс-ые) ионы ( см. гл. [27]
Таким образом, растворимость электролита уменьшается от введения в раствор одноименных ионов. Исключением являются те случаи, когда происходит связывание одного из находящихся в растворе ионов с вводимыми ионами в более сложные ( комплексные) ионы. [28]
Таким образом, растворимость электролита уменьшается от введения в раствор одноименных ионов. Исключением являются те случаи, когда происходит связывание одного из находящихся в растворе ионов с вводимыми ионами в более сложные ( комплексные) ионы ( см. гл. [29]
Таким образом, растворимость электролита уменьшается от введения в раствор одноименных ионов. Исключением являются те случаи, когда происходит связывание одного из находящихся в растворе ионов с вводимыми ионами в более ело / иные ( комплексные) ионы ( см. гл. [30]
Страницы: 1 2 3