Вводимый ион
Cтраница 3
Таким образом, растворимость электролита уменьшается от введения в раствор одноименных ионов. Исключением являются те случаи, когда происходит связывание одного из находящихся в растворе ионов с вводимыми ионами в более сложные ( комплексные) ионы ( см. гл. [31]
Увеличение концентрации вводимого иона вызывает обострение фронта ( границы) зон, если ион с меньшей валентностью вытесняет ион с большей валентностью. Уменьшение концентрации вводимого иона, наоборот, вызывает обострение фронта при вытеснении иона с меньшей валентностью или приводит к размыванию фронта при вытеснении иона с большей валентностью. [32]
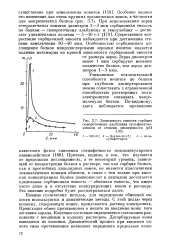 |
Зависимость емкости сорбции сывороточного альбумина сульфокатио-нптами от степени дисперсности ( рН. [33] |
Помимо статических методов, для определения обменной емкости используются и динамические методы. С этой целью через колонку, содержащую ионит, пропускается раствор электролита. Происходит обмен противоионов в ионите на вводимые ионы того же знака заряда. Конечное состояние определяется состоянием равновесия с вводимым в колонку раствором. Десорбируемые ионы выводятся из колонки. [34]
 |
Энергия взаимодействия Двух частиц. [35] |
Еще в 1890 - 1900 г. г. Шульце иГар - ди исследовали процессы коагуляции заряженных коллоидных частиц при добавлении электролитов. Эти авторы измеряли порог, коагуляции, или концентрацию электролита, При которой через определенный промежуток времени происходит коагуляция, добавляя анионы к коллоидным системам, содержащим положительно заряженные частицы, и катионы к коллоидным системам, содержащим отрицательно заряженные частицы. Эксперимент показал, 4то порог коагуляции зависит не от вида, а только от заряда вводимых ионов. [36]
Из табл. 2 видно, что дистиллят по сравнению с истинными растворами дает более широкую линию. Сужение линий ПМР природной воды ( общее солесодержание до 300 мг / л) и раствора бикарбоната кальция говорит о том, что вводимые ионы действуют разрушающим образом на квазикристаллическую структуру воды. Молекулы растворителя становятся более подвижными, более свободными. [37]
Для осуществления такого контроля проводимости требуется соблюдение некоторых важных условий. Ионы должны участвовать в процессе электронного обмена, так как, если этого не происходит, эффект сведется просто к появлению рассеивающего центра. Последнее часто происходит в тех случаях, когда добавляются жаростойкие окислы при температурах, при которых электронный обмен невозможен. Вводимый ион, кроме того, должен иметь более устойчивую электронную конфигурацию, чем ионы основной решетки. Например, в рассмотренном выше случае ионы лития обладают примерно теми же размерами, что и ионы никеля, но второй потенциал ионизации для лития составляет около 75 эв, в то время как третий потенциал ионизации никеля равен примерно 30 эв. В результате введение лития приводит к изменению валентности никеля. [38]
Увеличение концентрации вводимого она вызывает обострение фронта ( границы) зон, если ион с меньшей валентностью вытесняет ион с большей валентностью. Размывание фронта наблюдается, когда вытесняется ион с меньшей валентностью. Уменьшение концентрации вводимого иона, наоборот, вызывает обострение фронта при вытеснении иона с меньшей валентностью или приводит к размыванию фронта при вытеснении иона с большей валентностью. [39]
Собственно вантгоффит получают в двухзональном процессе с передачей потока из первой зоны во вторую и введением исходного сырья в обе зоны. Состав водной фазы в первой зоне поддерживают в пределах поля кристаллизации вантгоффита при 80 - 110 С. Конверсия в первой зоне ограничена выделением вантгоффита в качестве стабильной твердой фазы. Этого достигают ограничением концентрации побочного продукта конверсии MgCl2 значением 12 моль / 1000 моль Н20, вводимых ионов Mg2 и СГ, контролируя скорость перемещения потока из первой зоны во вторую. Во второй зоне в результате насыщения раствора хлоридом натрия и добавления некоторого количества сульфатсодержащего материала начинается рост кристаллов вантгоффита даже в том случае, если из-за понижения температуры фигуративная точка состава системы оказывается в поле кристаллизации левеита. [40]
Одной из форм существования коллоидов и полимеров является студнеобразное состояние, промежуточное между жидким и твердым состояниями. Застудневание коллоидных растворов - следствие нарушения агрегативной устойчивости, приводящее к структурообразованию. На процесс застудневания оказывают влияние концентрация раствора, форма частиц или молекул, температура, действие электролитов и ПАВ. Структурообразование в золях возможно только при определенной концентрации электролитов, которая резко уменьшается с увеличением заряда вводимых ионов. Ускорению застудневания растворов ВМВ способствуют небольшие концентрации электролитов. Высокие концентрации ПАВ препятствуют застудневанию, так как происходит полный разрыв связей между частицами. [41]
В связи с этим было интересно проследить за изменением коэффициентов диффузии обоих ионов при эквимолекулярном замещении друг другом. В качестве объекта исследования нами было выбрано стекло, содержащее 20 мол. Из нее видно, что особенно резкое изменение величины коэффициента диффузии происходит при введении в стекло первых количеств второй щелочи. Причем это характерно лишь для иона, концентрация в стекле которого подавляюща, величина же коэффициента диффузии вводимого иона меняется сначала очень незначительно. Нужно отметить, что, как и следовало ожидать, ион калия ввиду своего большого размера оказывает значительно большее влияние на величину коэффициента диффузии натрия, чем ион натрия на величину коэффициента диффузии калия. [42]
Наиболее эффективным методом обогащения воды серебром является электрохимическое растворение серебряного анода. Воздействие серебра на микробиальную клетку осуществляется в два этапа. Сначала происходит сорбция серебра на поверхности клетки, затем наблюдается проникновение его в клетку, что ведет к инактивации ферментов. Соединения серебра вызывают у кишечной палочки лизис цитоплазмы, повреждение нуклеотидов и отторжение содержимого клетки от оболочки. При концентрации серебра 0 1 - 0 2 мг / л кишечная палочка отмирает через 40 - 50 мин. Эффективность действия реагента зависит также от дозы вводимых ионов Ag и времени контакта с водой. Полное обеззараживание достигается при двухчасовом контакте. [43]
Страницы: 1 2 3