Галид
Cтраница 1
Галиды ВеС12, ВеВг2, Ве12 гигроскопичны и на воздухе расплываются; при их растворении в воде выделяется тепло; они растворимы также в органических растворителях. [1]
Галиды с катионами Си4, Ag и Аи практически нерастворимы в воде, за исключением фторида серебра AgF, который хорошо в ней растворяется. [2]
 |
Взаимосвязь меж - Устойчивость галидов одного и того же эле. [3] |
Галиды имеют разнообразное применение. Хлорид натрия, например, служит сырьем для получения хлора, едкого натра и др., хлорид и бромид серебра применяют в фотографии. Хлориды многих металлов и неметаллов используют для получения веществ высокой чистоты осаждением их из газовой фазы. Фторид серы SFB относится к лучшим газообразным диэлектрикам. [4]
Галиды обычно получают растворением оксидов или карбонатов в соответствующих галоводородных кислотах. [5]
Галиды 8.2 Гб представляют собой бесцветные жидкие или твердые вещества. Аналогичный бромид - 812Вг - плавится при 90 и кипит при 265 С, а иодид малоустойчив. Были также описаны продукты состава SiioCba ( вязкая жидкость), Si2oCl52 ( пластичная масса) и SiioClie. Последний из них имеет, по-видимому, бициклическое строение ( типа 4SiCl2 - 2SiCl - 4SiCl2) и представляет собой желтую, вазелиноподобную массу. [6]
Галиды - солеобразные вещества, трудноплавкие, образующие ионную кристаллическую решетку; в расплавленном состоянии - сильные электролиты; при электролизе их на отрицательном полюсе выделяется металл, на положительном - галоген. В воде они растворяются и диссоциируют на положительный ион металла и отрицательный ион галогена. [7]
Галиды Si2F6 представляют собой бесцветные жидкие или твердые вещества. Аналогичный бромид - Si2Br6 - плавится при 90 и кипит при 265 С, а иодид малоустойчив. [8]
Галиды и оксиды - металлов высшей степени окисления имеют неметаллический ( кислотообразующий) характер. [9]
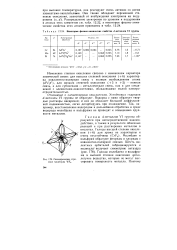 |
Некоторые физико-химические свойства - металлов VI группы.| Октаэдрическое строение молекулы WF6. [10] |
Галиды d - металлов VI группы образуются при непосредственном взаимодействии, а также в результате обменных реакций и при растворении металлов в кислотах. Молибден и вольфрам образуют фториды и хлориды с ковалентно-полярной связью. [11]
Галиды d - металлов I группы - солеобразные соединения, но при наличии свободных орбиталей у атомов, вступивших в соединение, легко переходят в комплексные соединения. [12]
Галиды и оксиды d - металлов высшей степени окисления имеют неметаллический ( кислотообразующий) характер. [13]
Галиды молибдена и вольфрама в высшей степени окисления представляют собой легколетучие вещества, которые не могут пассивировать поверхность металла. [14]
Галиды меди ( 2) имеют координационное число К. [15]
Страницы: 1 2 3 4