Галид
Cтраница 4
Галиды рассматриваемых элементов получаются непосредственным соединением металлов с галогенами или при растворении соответствующего гидроксида в галогеноводородной кислоте. В частности, хлорид платины PtCl2 образуется также при термическом разложении PtCl4; хлорид платины PtCl4 может быть получен при нагревании гексахлоро - ( 1У) платиновой кислоты Н2 [ PtClJ в атмосфере хлора при 300 С. [46]
Галиды более активных металлов имеют большую теплоту образования и более высокую температуру плавления. [47]
Галиды трехвалентных платиновых металлов характерны для рутения, родия, иридия и отчасти осмия. [48]
Ионные галиды наиболее активных металлов, являясь солями сильных кислот, не подвергаются гидролизу. [49]
 |
Растворимость водорода в железе и никеле в зависимости от температуры ( рн 1 013 105 Ли2. [50] |
Галидов высшей степени окисления железо не дает. [51]
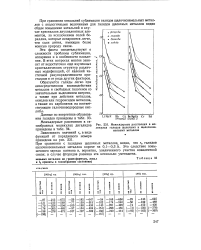 |
Межъядерные расстояния в молекулах галидов щелочных и щелочноземельных металлов. [52] |
Образуются галиды легко при непосредственном взаимодействии металлов и свободных галогенов со значительным выделением энергии, а также при действии металлов, окислов или гидроксидов металлов, а также их карбонатов на соответствующие галогеноводородные кислоты. [53]
Такие галиды классифицируются в той же товарной позиции, где и соответствующие кислоты. [54]
Страницы: 1 2 3 4