Галид - щелочной металл
Cтраница 1
Галиды щелочных металлов представляют собой соли, кристаллы которых обладают высокой степенью ионности и очень просты по своей структуре. [1]
 |
Модели газообразной. молекулы Nad. [2] |
Галиды щелочных металлов подобно рассмотренному LiF обладают также связями, обусловливаемыми участием нескольких а - и я-молекулярных орбиталей. [3]
Галиды щелочных металлов - соли, кристаллы которых обладают высокой степенью ионности и очень просты по структуре. [4]
 |
Схема фотоэлемента с внешним фотоэффектом. [5] |
Они напоминают галиды щелочных металлов. [6]
Комплексообразование с галидами щелочных металлов для рассматриваемых галидов ЭГа малохарактерно, но производные типов МЭГз и МаЭГ известны. [7]
При непосредственном образовании галидов щелочных металлов выделяются значительные количества энергии. Кристаллогидраты образует только Li - LiCl - 2H2O и, кроме фторидов, все соли гигроскопичны. Так, например, из галидов лития только LiF не изменяется при длительном хранении, а остальные соли расплываются. [8]
 |
Схема молекул оксида и пероксида натрия. [9] |
При непосредственном образовании галидов щелочных металлов выделяются значительные количества энергии. Кристаллогидраты образует только литий Li Cl 2Н2О, и, кроме фторидов, все соли гигроскопичны. [10]
При непосредственном образовании галидов щелочных металлов выделяются значительные количества энергии. Кристаллогидраты образует только литий LiCl - 2H2O, и, кроме фторидов, все соли гигроскопичны. [11]
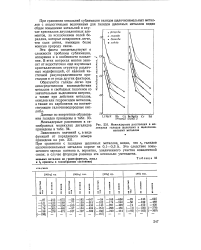 |
Межъядерные расстояния в молекулах галидов щелочных и щелочноземельных металлов. [12] |
При сравнении с галидами щелочных металлов видно, что тв галидов щелочноземельных металлов короче на 0 1 - 0 3 А. Это следствие повышенного заряда катиона и, вероятно, увеличенного участия ковалентной связи; в случае фторидов разница эта несколько уменьшена. [13]
Так как в кристаллах галидов щелочных металлов в большинстве случаев координационное число равно 6, а атом металла отдает не более одного электрона, перекрывание может дать максимально 1 / 6 электрона каждому соседнему атому галогена. Для достижения такого положения в сущности не надо заметно передвигать электрон по направлению от одного атома к другому в радиальном направлении. Скорее всего надо добиться неких изменений в азимутальном смысле: внешнее s - орбитальное облако атома катионогена должно из чисто сферического превратиться в искаженное шестью выступами, направленными к координированным атомам галогена. В случае явно ионных кристаллов можно приближенно предсказать межъядерное расстояние, складывая атомные ( а не ионные) радиусы максимальной плотности. Это свидетельствует о том, что даже в типично ионных структурах вклад ковалентного характера в волновую функцию достаточно велик для того, чтобы являться определяющим межъядерное расстояние. [14]
В дальнейшем проблема ионных структур будет рассмотрена в главе о галидах щелочных металлов, так как приведенных рассуждений еще недостаточно для понимания этого сложного вопроса. [15]
Страницы: 1 2 3