Галид - щелочной металл
Cтраница 2
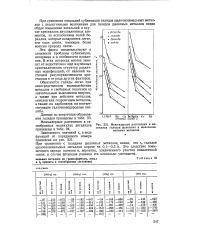 |
Межъядерные расстояния в молекулах галидов щелочных и щелочноземельных металлов. [16] |
При сравнении энтальпий сублимации галидов щелочноземельных металлов с аналогичными величинами для галидов щелочных металлов видно общее повышение энтальпий в случае кристаллов двухвалентных элементов, за исключением солей бериллия, которые испаряются легче, чем соли лития, имеющие более ионную природу связи. [17]
Однако экспериментальные данные свидетельствуют о связи, близкой к ионной лишь в галидах щелочных металлов. В рассмотренной молекуле MgO, например, на атомах проявляются заряды: 0 3, Mg 3 O 3 -, что никак не может отвечать описанному механизму ионной связи. [18]
Установлена линейность молекулы ( Li2O) и плоская ромбическая структура ( Li2O2), подобная димерам галидов щелочных металлов. [19]
 |
Структура алмаза.| Структура сфалерита. [20] |
Структурные типы NaCl и CsCl довольно широко распространены среди неорганических веществ, в частности структуры всех галидов щелочных металлов принадлежат к этим типам. [21]
 |
Кристаллическая решетка NaCl Светлые шары - ионы Na. темные - ионы Cl. [22] |
Структурные типы NaCl и CsCl являются довольно широко распространенными среди структур неорганических веществ, в частности, все галиды щелочных металлов имеют структуры, принадлежащие к этим типам. В обычных условиях решетку типа хлорида цезия имеют CsCl, CsBr и Csl, остальные галиды щелочных металлов имеют структуру типа NaCl. [23]
Однако в процессе развития теории химической связи было выяснено, что даже в типично ионных соединениях, например в галидах щелочных металлов, не происходит полного перехода электронов от одних атомов к другим. [24]
 |
Схема сопоставле.| Схема образования термов ( LiF из атомных термов Li и F. [25] |
На рис. 105 видно, что ковалентное перекрывание орбитальных сфер отступило на задний план, и ничто не мешает говорить, если не о чисто ионной связи, то во всяком случае, о взаимодействии, близком к обычной для галидов щелочных металлов модели. [26]
 |
Взаимосвязь меж - Устойчивость галидов одного и того же эле. [27] |
Тип химической связи, структура и свойства галидов зависят от химической природы как галогена, так и элемента, непосредственно с ним соединенного. Галиды щелочных металлов ( за исключением Li - Г), щелочноземельных металлов ( за исключением Be - Г), большинства лантаноидов и некоторых актиноидов относятся к ионным соединениям. [28]
Наглядное доказательство отсутствия полного разделения заряда в типичных ионных молекулах получено на основании измерений электрического момента диполя и межъядерных расстояний. Диссоциация галидов щелочных металлов на ионы в полярных растворителях объясняется тем, что ионы имеют большие энергии сольватации, способные скомпенсировать недостающую энергию диссоциации на ионы в газовой фазе. [29]
Электровалентная связь осуществляется в молекулах крайне редко. Она характерна для галидов щелочных металлов: атомы щелочных металлов характеризуются наименьшим ионизационным потенциалом, и атомы галогенов - наибольшим сродством к электрону. По-видимому, галиды двухвалентных металлов ( например, щелочноземельных) характеризуются также наличием электровалентной связи. [30]
Страницы: 1 2 3