Галид - щелочной металл
Cтраница 3
Недавно это было установлено опытным путем для многих галидов щелочных металлов. [31]
Структурные типы NaCl и CsCl являются довольно широко распространенными среди структур неорганических веществ, в частности, все галиды щелочных металлов имеют структуры, принадлежащие к этим типам. В обычных условиях решетку типа хлорида цезия имеют CsCl, CsBr и Csl, остальные галиды щелочных металлов имеют структуру типа NaCl. [32]
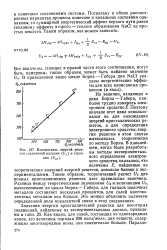 |
Взаимосвязь энергий решеток соединений кальция ( t / j и стронция ( Un. [33] |
Таким образом, теоретический расчет UQ для ионных кристаллических решеток дает правильные величины. Разница между теоретическими значениями UQ и величинами U0, вычисленными из цикла Борна - Габера, для галидов щелочных металлов составляет несколько процентов, для солей многовалентных металлов она больше. [34]
Влияние дислокаций и других дефектов сказывается не только на росте кристалла и его механических свойствах, но и на электрических свойствах полупроводников, так как вызывают рассеяние носителей заряда. Дефекты решетки сильно влияют на оптические свойства некоторых кристаллов. Например, вакансии в анионной подрешетке галидов щелочных металлов являются центрами притяжения электронов. Когда в места таких вакансий попадают электроны, то возникают так называемые F-центры, вследствие чего бесцветные прозрачные кристаллы ( NaCl и др.) приобретают синюю или пурпурную окраску из-за поглощения света электронами, захваченными дефектами решетки. [35]
Самая большая ЭО у галогенов, самая малая - у щелочных металлов. Естественно предположить, что ионная связь наиболее вероятна именно между атомами галогенов и атомами щелочных металлов. Эксперимент подтверждает распределение электронной плотности по ионному образцу в ряде галидов щелочных металлов. [36]
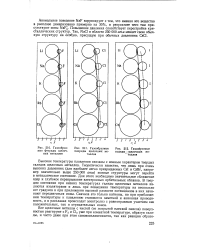 |
Газообразные фториды щелочных металлов.| Газообразные хлориды щелочных металлов.| Газообразные иодидьг щелочных ме - таллов. [37] |
Высокие температуры плавления связаны с ионным характером твердых галидов щелочных металлов. Теоретически известно, что лишь при очень высоких давлениях ( для наиболее легко превращаемых Csl и CsBr, например значительно выше 250 000 атм) ионные структуры могут перейти в металлическое состояние. Для этого необходимо значительное сближение ядер и глубокое перекрывание электронных орбитальных облаков. В твердом состоянии при низких температурах галиды щелочных металлов являются изоляторами и лишь при повышении температуры на несколько сот градусов и при приложении высокой разности потенциалов в них начинают передвигаться ионы. Сначала это только катионы, но при приближении температуры к плавлению становится заметной и анионная проводимость, а в расплавах происходит электролиз с равноправным участием как положительных, так и отрицательных ионов. [38]
Структурные типы NaCl и CsCl являются довольно широко распространенными среди структур неорганических веществ, в частности, все галиды щелочных металлов имеют структуры, принадлежащие к этим типам. В обычных условиях решетку типа хлорида цезия имеют CsCl, CsBr и Csl, остальные галиды щелочных металлов имеют структуру типа NaCl. Недавно это было установлено опытным путем для многих галидов щелочных металлов. [39]
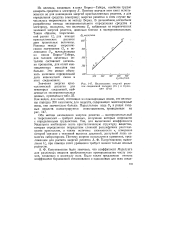 |
Взаимосвязь энергий решеток соединений кальция ( Ui и стронция ( / ц. [40] |
Поэтому вначале этот цикл использовался не для нахождения энергий кристаллических решеток, а для определения сродства электрону; энергия решетки в этом случае вычислялась теоретически по методу Борна. В дальнейшем, когда были разработаны методы экспериментального определения сродства к электрону, оказалось, что величины Е, найденные из теоретических значений энергий решеток, довольно близки к экспериментальным. Таким образом, теоретический расчет U0 для ионных и ккал / мом кристаллических решеток дает правильные величины. Разница между теоретическими значениями Uu и величинами U0, вычисленными из цикла Борна-Габера, для галидов щелочных металлов составляет несколько процентов, для солей многовалентных металлов она больше. [41]
Страницы: 1 2 3