Гало-геноводород
Cтраница 1
Гало-геноводороды легко реагируют с А. [1]
Гало-геноводороды обычно присоединяются к кратным связям как электрофильные реагенты. [2]
Гало-геноводороды обычно присоединяются к кратным связям как электрофильные реагенты. Однако с эфирами ацетиленкарбоно-вых кислот, где электрофильное присоединение затруднено в результате сильного электроноакцептопного воздействия карбоксильных групп, реакция идет как нуклеофильный процесс. [3]
 |
Контактная печь для реакций проточным методом. [4] |
Отщепление двух молекул гало-геноводорода от 1 2-дигалогензаме-щенных может, в зависимости от строения углеводородного остатка, привести либо к алкадиенам, либо к ацетиленам. [5]
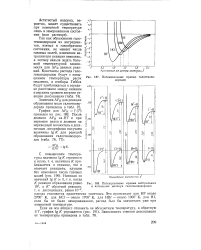 |
Потенциальные кривые галогеново-дородов.| Потенциальные кривые нейтральных и катионных молекул галогеноводородов. [6] |
Так как образование гало-геноводородов из ингредиентов, взятых в газообразном состоянии, не меняет числа газовых молей, изменение энтропии при реакции невелико, а потому нельзя ждать большой температурной зависимости для А / н данных реакций. [7]
Объясните электронный механизм присоединения гало-геноводородов по правилу Марковникова. [8]
При взаимодействии диенов с гало-геноводородами также образуется смесь продуктов 1 2 - и 1 4-присоединения; их соотношение также зависит от условий проведения реакции. Так, При гидробромировании бутадиена-1 3 ( рис. 1.2) выходы соединений ( 78) и ( 79) при - 80 С составляют 80 и 20 % соответственно, а при 40 С они равны 20 н 80 % соответственно. [9]
При взаимодействии диенов с гало-геноводородами также образуется смесь продуктов 1 2 - и 1 4-присоединения; их соотношение также зависит от условий проведения реакции. Так, при гидробромировании бутадиена-1 3 ( рис. 1.2) выходы соединений ( 78) и ( 79) при - 80 С составляют 80 и 20 % соответственно, а при 40 С они равны 20 и 80 % соответственно. [10]
Хлорангидриды кислот, галогены, гало-геноводороды, метилхлорметиловый эфир и метилхлорметилсуль-фид также расщепляют 1 1-диамины, давая а-галогенамины R R2NCH2C1 ( см. разд. [11]
Определенные калориметрическим методом теплоты растворения гало-геноводородов в воде при 291 К. [12]
Гидроксил спирта заменяется галогеном при действии гало-геноводорода или галогенидов фосфора. [13]
Кислоты Льюиса также повышают реакционную способность гало-геноводородов по отношению к двойным связям. [14]
В некоторых случаях после окислительного присоединения гало-геноводорода протекает дальнейшая реакция. При реакции внутри-сферного гидридного лиганда со свободными протонами образуется газообразный водород. [15]
Страницы: 1 2 3 4