Галоген-анион
Cтраница 1
Галоген-анион в ионной паре может выступать в роли внутреннего нуклеофнла, и при росте основности Hal вероятность отщепления должна увеличиваться. [1]
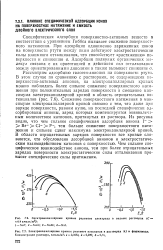 |
Электрокапилляриые кривые ртутного электрода в растворах KI в формамнде. [2] |
Рассмотрим адсорбцию галоген-анионов на поверхности ртути. Снижение поверхностного натяжения в максимуме электрокапиллярной кривой связано с тем, что даже при заряде поверхности, равном нулю, на последней специфически адсорбированы анионы, заряд которых компенсируется эквивалеч. Из рисунка видно, что чем сильнее специфическая адсорбция аниона 1 - Вг - С1 - F -, тем больше снижение поверхностного натяжения и сильнее сдвиг максимума электрокапиллярной кривой. В области отрицательных зарядов поверхности все кривые сливаются, что обусловлено десорбцией анионов и электростатическим взаимодействием катионов с поверхностью. [3]
Потенциометрическое титрование галоген-аниона, при кото ром галогенобензол не титруется, является мерой образования дегидробензола. [4]
Из значений поляризуемости галоген-анионов можно установить, что электроны удерживаются тем менее прочно, чем тяжелее галоген. [5]
Алкилгалогениды образуют карбо-ниевые ионы путем отщепления галоген-аниона. Однако первичные и вторичные алкилгалогениды малоактивны; только с третичными алкилгалогенидами можно получить приемлемые выходы. [6]
Реакция происходит, вероятно, благодаря атаке галоген-анионом, причем образуется изображенное ниже промежуточное соединение, которое затем циклизуется в конечный продукт. [7]
Механизм ацилирования спиртов ангидридами аналогичен механизму реакции с применением хлорангидри-дов, только в данном случае происходит отрыв не галоген-аниона, а аниона-карбоксилата. [8]
Лоренц [69-71] предполагает образование такой связи, эквивалентное переносу части заряда адсорбированного иона на металл, при адсорбции галоген-анионов и катионов калия и цезия на ртутном и галлиевом электродах. [9]
Таким образом, энергетический барьер между различными изомерными неклассическими ионами оказывается выше, чем энергия активации реакции с галоген-анионом. [10]
 |
Карбонилирование галогензамещенных олефинов. [11] |
В жестких условиях кислоты могут быть получены и из насыщенных галогенпроизводных591, Алкилгалогениды образуют карбо-ниевые ионы путем отщепления, галоген-аниона. Однако первичные и вторичные алкилгалогениды малоактивны; только с третичными алкилгалогенидами можно получить приемлемые выходы. [12]
Энергия сольватации ионов при переходе из газовой фазы в воду ( от - 60 до - 120 ккал / моль для галоген-анионов [65]) превышает на несколько порядков те относительно небольшие различия в свободной энергии активации, которые следуют из наблюдаемых скоростей реакций. [13]
Образование связи между нуклеофилом и р-углеродным атомом дает тетраэдри-яески построенный карбанион, в котором пространство, предназначенное для одной из валентностей а-угяеродного атома, занимает свободная электронная пара, что является результатом йгракс-присоединения галоген-аниона и электронной пары. [14]
Тем не менее амфионный ( цвиттерионный) механизм, возможно, имеет значение для тех систем, в которых пространственные барьеры замедляют замыкание кольца в нормальном направлении и, таким образом, позволяют галоген-аниону отойти за пределы стереоселективного электростатического взаимодействия, прежде чем образуется новая связь. [15]
Страницы: 1 2 3