Галоген-анион
Cтраница 2
Тем не менее амфиопный ( цпиттерионный) механизм, тюзможно, имеет значение для тех систем, в которых пространственные барьеры замедляют замыкание кольца в нормальном ( вправлении и, таким образом, позволяют галоген-аниону отойти за пределы стереоселектииного электростатического взаимодей-стния, прежде чем образуется новая снизь. [16]
Образование связи между нуклеофилом и - углеродным атомом дает тетраэдри-ческн построенный карбанион, в котором пространство, предназначенное для одной из валентностей - углеродного атома, занимает свободная электронная пара, что является результатом транс-присоединения галоген-аниона и электронной пары. [17]
Во всех приведенных выше примерах присоединения несимметричных реагентов к двойной связи, углеродные атомы которой связаны с неодинаковым числом атомов водорода, присоединяющийся водород направлялся к тому из углеродных атомов, у которого уже имеется большее число водородных атомов, а анионная часть молекулы ( галоген-анион, остаток серной кислоты, гидроксил воды) - к соседнему атому углерода. Это проявление одного из наиболее известных правил, созданных в свое время В. В. Марков-никовым; именно этому правилу и присвоено имя открывшего его ученого. [18]
Промежуточные соединения, приводящие к продуктам реакции, являются, по-видимому, неклассическими карбокатионами. Атака галоген-анионом происходит стереоопецифично, вопреки стеричеоким факторам, в соответствии со строением промежуточных неклассических ионов. [19]
Такой порядок характерен для апротонных диполярных растворителей моноглима и диметилацетамида. Нарушение порядка нуклеофильности галоген-анионов возможно в системе метиловый спирт - диоксан ( 1: 20), в которой содержание протонного растворителя незначительно и к тому же электрофйльность метилового спирта существенно ослаблена в результате образования водородной связи с диоксаном. [20]
При растворении соли происходит также взаимодействие растворенных частиц с растворителем. Например, в апротонных растворителях степень сольватации галоген-анионов обратна той, которая наблюдается в водных растворах и, например, в диметилформами-де ионы хлора оказываются несольватированными. Понижение диэлектрической проницаемости приводит к усилению взаимодействия между катионами и анионами, что вызывает увеличение констант устойчивости комплексных соединений. Все эти явления коренным образом изменяют состав раствора по сравнению с составом водного раствора, содержащего те же концентрации растворенных солей. Растворитель также не является инертной средой, он входит во внутреннюю координационную сферу комплексов и адсорбируется на поверхности твердого электрода. [21]
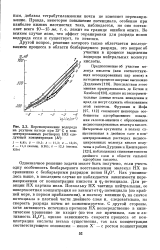 |
Перенапряжение водорода на ртутном катоде при 25 С в концентрированных растворах НС1 следующей концентрации ( М. [22] |
Впоследствии этого мнения придерживались де Бетюн и Кимболл [120], однако их экспериментальные данные весьма ненадежны и вряд ли могут служить обоснованием этой гипотезы. Фрумкин и Иофа [97, 112] связывают некоторые особенности адсорбционного поведения галоген-анионов с образованием недиссоциированных молекул кислот. Интересные аргументы в пользу существования в двойном слое в кон - центрированных растворах недиссоциированных молекул кислот получены в работе Дур дина и Цвентарного [121], наблюдавших снижение емкости двойного слоя в области сильной адсорбции кислоты. [23]
Наиболее распространенной реакцией этого типа является щелочная эпокси-дация с отщеплением гидроксил-аниона. Карбонионные нуклеофилы, содержащие галоген, могут давать циклоалканы с отщеплением галоген-анионов в стадии циклизации. Что касается азотсодержащих нуклеофилов, то даже при наличии способных к отщеплению групп они не образуют циклических соединений ( азиридинов) в результате непосредственного взаимодействия. [24]
Уменьшение сольватации анионов повышает их реакционную способность в 5 2-реакциях, причем тем больше, чем меньше объем аниона. Поэтому в растворителях, не способных к специфической сольватации анионов, наблюдается изменение порядка ну-клеофильности галоген-анионов по сравнению с протонными растворителями. [25]
Как и хлорангидриды кислот, ангидриды кислот широко применяют для получения сложных эфиров из соединений, содержащих оксигруппу. Механизм этой реакции такой же, как и при реакции с хлор ангидрид ом кислоты, только при этом происходит отрыв аниона кар боксилата, а не галоген-аниона. [26]
Во-первых, металл может быть просто катализатором; во-вторых, металл может служить источником электронов для связи С - X, что облегчит удаление галогена в виде галоген-аниона, и, в-третьих, металл может образовать металлоорганическое соединение, в котором металл: может быть связан с атомом углерода связью, либо преимущественно кова-лентной, либо преимущественно ионной. [27]
Разнообразные реакции галогенпроизводных, включающие использование металлов, либо в виде элементов, либо в виде соединений, удобно разделить на три группы. Во-первых, металл может быть просто катализатором; во-вторых, металл может служить источником электронов для связи С - X, что облегчит удаление галогена в виде галоген-аниона, и, в-третьих, металл может образовать металлоорганическое соединение, в котором металл может быть связан с атомом углерода связью, либо преимущественно кова-лентной, либо преимущественно ионной. [28]
Предполагается, что одна из трех неподеленных пар электронов галогена принимает участие в образовании связи с развивающимся карбониевым ионом, образуя хлорониевый, бром-ониевый или иодониевый катион с трехчленным кольцом, и таким образом предотвращается вращение водорода вокруг С-С - связи. Геометрическое расположение галониевого иона, где все четыре заместителя первоначальной двойной связи находятся в одной плоскости, перпендикулярной к плоскости образующегося трехчленного цикла, облегчает последующую реакцию с галоген-анионом. Эта реакция связана с обращением конфигурации атакуемого атома углерода. Таким образом, гранс-олефины дают 1 2-дигалогенпроизводные с эригро-конфигурацией, а цыс-оле-фины - соединения с rpeo - конфигурацией. [29]
В случае галогенпроизводных или арилсерных эфиров образующийся анион очень устойчив и даже неспецифические взаимодействия с растворителем иногда оказывают достаточно сильное стабилизующее влияние, так что ионные механизмы становятся преобладающими. Примером этого может служить мономолекулярный сольволиз трет-алкилгалогенидов и п-толуолсуль-фонатов в водно-спиртовых средах. Однако гораздо большая степень стабилизации возможна для случаев специфического взаимодействия галоген-анионов с компонентами среды. [30]
Страницы: 1 2 3