Галогеналкила
Cтраница 1
Галогеналкилы обладают значительной полярностью. [1]
Галогеналкилы применяются в качестве алкили-рующих средств ( см. с. Наибольшей активностью при этом обладают йодистые соединения. [2]
Галогеналкилы обладают большей реакционной способностью по отношению к магнию, чем гало-генарилы. В алифатическом ряду на выход реактива Гриньяра оказывает влияние величина и разветвленность радикала: реакционная способность снижается с удлинением или разветвлением цепи. С хорошими выходами получаются обычно магнийорганиче-ские соединения из галогенопроизводных циклопарафинового ряда и ароматических соединений с галогеном в боковой цепи. Ароматические соединения, имеющие галоген в ядре, например бромбензол и иодбензол, образуют реактивы Гриньяра с хорошими выходами. Увеличение числа заместителей ( метальных, метоксильных групп) в ядре вызывает затруднения в приготовлении магнийорганических соединений. Галогенопроизводные конденсированных циклов, например, а - и ( J-бромнафталины, нормально реагируют с магнием в большинстве случаев. [3]
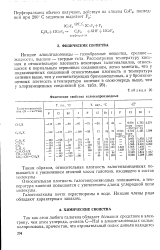 |
Физические свойства галогенпроизводных. [4] |
Галогеналкилы почти нерастворимы в воде. Низшие члены ряда обладают характерным запахом. [5]
Галогеналкилы в обычных условиях не взаимодействуют с силаном, а галогенацилы ведут себя аналогично галогенводородам. [6]
Галогеналкилы обладают большей реакционной способностью по отношению к магнию, чем гало-генарилы. В алифатическом ряду на выход реактива Гриньяра оказывает влияние величина и разветвленность радикала: реакционная способность снижается с удлинением или разветвлением цепи. С хорошими выходами получаются обычно магнийорганиче-ские соединения из галогенопроизводных циклопарафинового ряда и ароматических соединений с галогеном в боковой цепи. Ароматические соединения, имеющие галоген в ядре, например бромбензол и иодбензол, образуют реактивы Гриньяра с хорошими выходами. Увеличение числа заместителей ( метильных, метоксильных групп) в ядре вызывает затруднения в приготовлении магнийорганических соединений. Галогенопроизводные конденсированных циклов, например, а - и 5-бромнафталины, нормально реагируют с магнием в большинстве случаев. [7]
Галогеналкилы не диссоциируют на ионы, поскольку атомы галогена связаны с радикалом не ионной связью, а ковалентной. [8]
Галогеналкилы почти нерастворимы в воде. [9]
Галогеналкилы образуют с хорошими выходами ртутьдиалкилы уже на холоду, а галогенарилы - при нагревании. Обычно лучшие выходы ртутьорганических соединений получаются при использовании иодпроизводных углеводородов, однако сравнительно недавно Мельниковым [204, 223] было показано, что ртутьдиалкилы с хорошими выходами могут быть получены при использовании бромзамещенных алифатических углеводородов. В качестве необходимого катализатора этой реакции обычно применяют уксусно - - этиловый или уксуснометиловый эфир. [10]
Галогеналкилы образуют с хорошими выходами ртутьди-алкилы уже на холоду, а галогенарилы - при нагревании. Обычно лучшие выходы ртутьорганических соединений получаются при использовании йодистых производных углеводородов, однако сравнительно недавно Мельниковым было показано [302], что ртутьдиалкилы с хорошими выходами могут быть получены при использовании бромзамещенных алифатических углеводородов, если реакцию проводить при интенсивном перемешивании и низкой концентрации амальгамы. В качестве необходимых катализаторов этой реакции обычно применяются уксусноэтиловый, или уксуснометиловый эфи-ры. При этих условиях удается получать с довольно высокими выходами диметилртуть, диэтилртуть, дипропилртуть, дибутилртуть, диизобутилртуть, диизоамилртуть. [11]
Галогеналкилы, так же как и С12 или НС1, при повышенных ( Температурах, вероятно, могут хлорировать А12Оз, превращая ее в А1С13, подобно тому, как это происходит под действием TiCU. [12]
Галогеналкилы имеют большое значение в качестве исходных продуктов для реакций Гриньяра ( стр. [13]
Галогеналкилы и галогеноводородные кислоты в реакциях с 1М К-алкил-аминоарсинами также расщепляют As-N связь. [14]
Галогеналкилы с большим числом углеродных атомов имеют еще большее количество изомеров. [15]
Страницы: 1 2 3 4