Галогенид-ион
Cтраница 1
Галогенид-ион в транс-положении к гидрид-иону может быть замещен нейтральной донорной молекулой с образованием нового катионного гидридного комплекса. Активирующее влияние координированного гидрид-иона в этом случае является очень важным фактором. [1]
Какой галогенид-ион является самым активным восстановителем. [2]
Способность галогенид-ионов увеличивать адсорбцию органических веществ является очевидно, универсальной для соединений которые находятся в электролите в виде катионов. [3]
Из галогенид-ионов наиболее сильный эффект оказывали иодид и бромид-ионы. Защитные свойства серусодержащих неорганических соединений ЫагЭгОз, Na2S03 и Na2S примерно одинаковы. [4]
Концентрация галогенид-ионов также является существенным фактором, влияющим на эффективность концентрирования. [5]
Присоединение галогенид-иона к этому интермедиату дает конечный продукт, Детальное изучение стереохимии хлорирования конформационно жестких циклических сульфоксидов подтвердило этот механизм. [6]
Кроме галогенид-ионов хорошими уходящими группами являются, например, тозилат-анион ( ср. [7]
Источником галогенид-иона в таких случаях является водный раствор галогенида щелочного металла. [8]
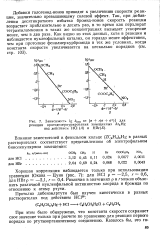 |
Зависимость lg. отн от. [9] |
Добавки галогенид-ионов приводят к увеличению скорости реакции, значительно превышающему солевой эффект. Так, при добавлении десятикратного избытка бромид-ионов скорость реакции возрастает приблизительно в десять раз, в то время как перхлорат тетраэтиламмония в таких же концентрациях вызывает ускорение менее, чем в два раза. Как видно из этих данных, хотя в реакции и наблюдается нуклеофильный катализ, он гораздо менее эффективен, чем при протолизе фенилмеркурбромида в тех же условиях, когда константа скорости увеличивается на несколько порядков ( см. стр. [10]
Адсорбция галогенид-ионов изменяет кинетику и механизм процесса анодного растворения железа. В зависимости от концентрации галоге-ниды могут как ингибировать, так и стимулировать процесс. Чаще всего предполагается последовательное присоединение к поверхностным атомам железа гидроксид - и галогенид-ионов. При этом принимается, что образуются сложные адсорбированные продукты типа [ Fe ( OH) ( X -) ] аде, где Х - - галогенид-ион. [11]
Количество галогенид-иона, элиминированного в реакции при соотношении реагентов 1: 1: 4, показывает, что в этих условиях реакция может не доходить до конца. Предполагается, что причиной этого может быть нерастворимость замещенных продуктов, а также их разложение. [12]
Замена галогенид-иона в галогензамещенных соединениях ал-коксигруппами моделирует многие реакции, включая широко распространенный синтез Вильямсона, замещение сульфогрупп, метод Ульмана, внутримолекулярное замещение, приводящее к образованию циклических эфиров, в том числе метод Дарзана, а также вытеснение третичных аминов из четвертичных оснований. [13]
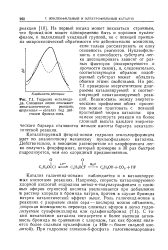 |
Гидролиз метилиоди - ций. Взаимосвязь между энергети-да. Сплошная линия описывает ческими профилями обоих процес-екаталитическую реакцию, CQB трактовать С позиций. [14] |
Катализ галогенид-ионами наблюдается и в катализируемых кислотами реакциях. Например, скорость катализируемого хлорной кислотой гидролиза метил-п-толуолсульфината и слож-вых эфиров сернистой кислоты увеличивается при добавлении в раствор хлорида и бромида натрия, причем в случае бромида натрия каталитический эффект выше. [15]
Страницы: 1 2 3 4