Галогенид-ион
Cтраница 2
Прямое определение галогенид-ионов основано на окислении их на платиновом или графитовом электродах. До сих пор не было опубликовано работ по прямому использованию хронопотенциометрии для определения фторид-иона. [16]
Различное влияние галогенид-ионов на ртуть и железо показывает, что переносить закономерности, установленные для систем, в которых электрод - ртуть, на системы с твердыми металлами в качестве электродов, надо с большой осторожностью. [17]
Специфическая адсорбция галогенид-ионов общеизвестна. Она наблюдается для большинства металлов и так же, как и для ртути, отражает наличие некоторого химического взаимодействия. В достаточно концентрированных растворах адсорбционные потенциалы в присутствии анионов С1 - и Вг - достигают высоких значений и на границе с воздухом. [18]
Косвенное определение галогенид-ионов с ксиленоловым оранжевым основано на титровании раствором азотнокислого серебра в присутствии комплексов диэтилдитиокарбамата свинца при титровании хлорид-ионов и диэтилдитиокарбамата висмута при титровании бромид - и иодид-ионов. При незначительном избытке серебра освобождающиеся ионы РЬ ( П) и Bi ( III) взаимодействуют с ксиленоловым оранжевым. [19]
Если концентрация галогенид-ионов существенно больше, чем галогена, то при сВГ2 0 1 М взаимодействие между ними приводит к образованию иона Вгз - Его константа устойчивости в растворах Li, НСЮ4 с общей концентрацией 3 М, [ Н ] 0 1 г-ион / л и температуре 25 С, по данным экстракционного, калориметрического и спектрофотометрического методов, найдена соответственно равной 11 3 1 4, 11 1 0 3 и 12 7 0 3 [165]; близость полученных величин указывает на их достоверность. [20]
 |
Состав продуктов реакции СНВг2С1 с различными алкенами в стандартных условиях ( катализатор ТЭБА. [21] |
Локальная концентрация постороннего галогенид-иона должна быть очень мала, поскольку концентрация ТЭБА невелика. Для смешанных галоформов можно-ожидать более высокие локальные концентрации различных га-логенидов и, возможно, благоприятные условия для процессов, обмена. [22]
Последовательное окисление упомянутых галогенид-ионов, которое лежит в основе их обнаружения раствором КМпО4, начинается лишь после окисления им тиосульфат-ионов. [23]
Наряду с галогенид-ионами электронными мостиками могуг быть цианид - и сульфат-ионы, молекулы воды и даже сравнительно большие анионы карбоновых и дикарбоновых кислот. [24]
С каким галогенид-ионом Со3 образует относительно устойчивое соединение. [25]
С каким галогенид-ионом СО3 образует относительно устойчивое соединение. [26]
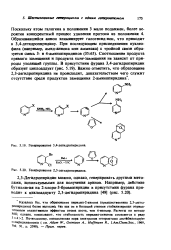 |
Генерирование 3 4-дегидропнрнднна.| Генерирование 2 3-дегндропнрндина. [27] |
Образовавшийся анион элиминирует галогенид-ион, что приводит к 3 4-дегидропиридину. Соотношение продукта прямого замещения и продукта кине-эамещения не зависит от природы уходящей группы. [28]
Если X - галогенид-ион и L-амин, то карбонат вступает в комплекс, вытесняя X по внутримолекулярному механизму. [29]
В растворе содержались галогенид-ион и белое твердое вещество, которое давало положительную реакцию на бораты. [30]
Страницы: 1 2 3 4