Галогениды
Cтраница 2
Галогениды ЭГ2 - кристаллические вещества ( BeF2 существует также в виде стекловидной массы), большинство из них очень хорошо растворяется в воде ( практически нерастворимы фториды Mg, Ca, Sr, Ba); образуют кристаллогидраты. Обычно безводные ЭГ2 получают, нагревая кристаллогидраты этих солей в токе галогеноводорода. [16]
Галогениды РЬГ2 малорастворимы в холодной воде. Растворимость ярко-желтого РЫ2 сильно возрастает с повышением температуры. При медленном охлаждении нагретого раствора дииодид свинца выделяется в виде ярких блестящих золотистых кристаллов, которые долго удерживаются во взвешенном состоянии - это вещество легко отличить от всех других. [17]
Галогениды, оксогалогениды и оксиды Э ( VI) являются кислотными с некоторыми признаками амфотерности. Им соответствуют анионные комплексы. [18]
 |
Схема строения молекулы Р4Ов. [19] |
Галогениды Р ( III) легко вступают в донорно-акцептор-ное взаимодействие с соединениями, являющимися акцепторами электронных пар. [20]
Галогениды реагируют подобным же образом. [21]
Галогениды сульфурила, SO2X2, являются еще одним примером шестивалентных тетраэдрических молекул с двумя я-связями. Например, в сульфурилфториде ( 64 Г) углы OSO и FSF равны соответственно 124 и 96 1, а расстояния S-О ( 143 пм) соответствуют длинам двойных связей. [22]
Галогениды и оксигалогениды плутония используются на различных стадиях технологического процесса получения плутония. Имеются также указания на применение галогенидов для разделения актинидных элементов. Описан метод [314] отделения летучего гексафторида урана от гексафторида плутония. [23]
Галогениды природные - группа минералов, соединения галогенов ( фтора, хлора, брома, йода) с другими химическими элементами. В природе наиболее распространены хлориды ( ок. [24]
Галогениды алкильных производных алюминия получают фракционированием смеси соединений, образующихся при растворении металлического алюминия в алкилгалогенидах. [25]
Галогениды алкильных производных алюминия представляют собой тугоплавкие легко растворимые ( димерные в растворах) соединения, бурно реагирующие с кислородом и влагой воздуха. [26]
Галогениды, соответствующие высшим степеням окисления, обладают ковалентными связями, они легко летучи, растворимы в органических растворителях и гидролизуются водой. Соединения двухвалентного рения малочисленны, они менее устопчивы и имеют менее выраженные восстановительные свойства, чем соединения двухвалентного марганца. Соединения трех -, четырех - п шестивалентпого рения более устойчивы, чем соответствующие соединения марганца. [27]
Галогениды сульфония ( подобно аммониевым солям) с влажным оксидом серебра образуют сульфо-ниевые основания. [28]
Галогениды и галогенидподобные ионы [ CN -, N3, ООС -, CNO -, SeCN -, N ( CN) 2 - и др. ] играют важную роль в при-электродных процессах, особенно в случаях, когда заряд электродов по отношению к растворам положителен. Адсорбируясь на катоде ( например, Си, Ag, Аи), эти ионы деполяризуются по мостиковому механизму. [29]
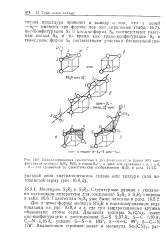 |
Идеализированная ( валентные и диэдрические углы равны 90 кон. [30] |
Страницы: 1 2 3 4