Водородный ион
Cтраница 1
 |
Некоторые полимеры фтористого водорода. [1] |
Водородный ион, создающий водородную связь, обычно прочнее связан с одним из двух электроотрицательных атомов, которые он удерживает вместе. [2]
Водородные ионы, отличающиеся особенно высокой теплотой гидратации, в безводных кислотах, по крайней мере в большинстве случаев, если не всегда, связаны более гомеополярно, чем гетерополярно, и эта гомеополярная связь имеет заметно отличающуюся от нуля ионность ( см. стр. [3]
Водородные ионы повышают скорость коррозионных процессов и одновременно уменьшают прочность защитной оксидной пленки на поверхности металла. [4]
Водородные ионы содержатся в почвах обычно в адсорбированном виде. Поэтому для выявления кислотности почвы химическим путем, с помощью индикаторов, почва взбалтывается не с чистой водой, а с раствором хлористого калия, катионы которого вытесняют ионы гидроксония из адсорбционного слоя. [5]
Водородные ионы вытесняют слабую кислоту, двуокись углерода, из соединения с оксид-ионом. Другим примером, описанным у Льюиса [1], является выделение двуокиси углерода при нагревании тонко измельченного карбоната натрия с хлористым бором или хлорным оловом в смеси четыреххлористого углерода с ацетоном. [6]
Водородные ионы, идущие на образование молекул воды, отщепляются от недиссоциирующих молекул уксусной кислоты только в процессе реакции нейтрализации, тогда как гидроксильные ионы, образовавшиеся за счет практически полной диссоциации едкого натра, существуют в растворе до начала реакции самостоятельно. [7]
Водородные ионы, необходимые для ее образования, существуют в растворе сильной серной кислоты в свободном состоянии. [8]
Водородные ионы, необходимые для ее образования, существуют в растворе сильной серной кислоты в свободном состоянии. Что же касается гидроксильных ионов, то они входят в состав практически недиссоциирующего слабого основания, гидроокиси серебра, и приходят во взаимодействие с водородными ионами серной кислоты только во время реакции. [9]
Водородные ионы известны как катализаторы разнообразных гетеролитических реакций, в том числе и гетеролитическо-го распада перекисей. Недавно было показано [105], что сильные минеральные кислоты ускоряют окисление изопропи-лового спирта, разрушая Н2О2 на свободные радикалы. [10]
Водородные ионы, ионы высшей валентности, как, например, А1, Fe, Са и многие другие, не только способны весьма сильно понизить величину g - потен-циала, но и вызвать уже при незначительной концентрации ионов перемену его знака. Объясняется это тем, что отдельные ионы обладают по отношению к поверхности твердой фазы не только электрическим, но и адсорбционным потенциалом, выражающимся работой, затрачиваемой на перевод одного моля катионов или анионов из глубины раствора в мономолекулярный слой на границе раздела двух фаз. [11]
Водородные ионы в водных растворах благодаря своей большой подвижности занимают особое положение. Они служат катализаторами для многих химических реакций, определяют направление разнообразных физико-химических и многих биохимических процессов и, несомненно, являются одним из существенных факторов в жизни озер и при формировании соляных отложений. [12]
Водородные ионы могут вызывать еще один отрицательный эффект, опять-таки сходный с механизмом воздействия некоторых отрицательных модуляторов на ферментативный катализ. Это влияние рН на кислородную емкость гемоглобина называют эффектом Рута. Сильно выраженный эффект Рута часто сопутствует большому эффекту Бора. [13]
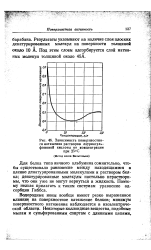 |
Зависимость поверхностного натяжения растворов лаурилсуль-фоновой кислоты от концентрации при 25 С. [14] |
Водородные ионы вообще имеют резко выраженное влияние на поверхностное натяжение белков; минимум поверхностного натяжения наблюдается в изозлектриче-ской области. [15]
Страницы: 1 2 3 4