Безводные галогениды
Cтраница 4
При обезвоживании галогениды частично гидролизуются. Не содержащие кристаллизационной воды галогениды магния и кальция ( кроме фторидов) гигроскопичны: поглощают пары воды из воздуха. Безводные галогениды термически устойчивы. [46]
 |
Взаимосвязь между стандартными энтальпиями реакции Э ( ОН2 ( к COg ( г. [47] |
Обычно безводные ЭГ2 получают, нагревая кристаллогидраты этих солей в токе галогенводорода. Еще более подвержены гидролизу галогениды бериллия. Безводные галогениды Be получают, действуя Г2 или НГ на металл при высокой температуре. [48]
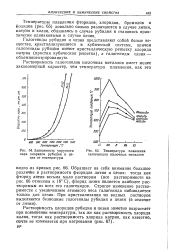 |
Зависимость упругости.| Температура плавления галогенидов щелочных металлов. [49] |
Обращает на себя внимание большое различие в растворимости фторидов лития и цезия: тогда как фторид лития весьма мало растворим ( все растворимости на рис. 66 отнесены к 18 С), фторид цезия является наиболее растворимым из всех его галогенидов. Строгое изменение растворимости с увеличением атомного веса галогенида наблюдается только для цезия. При кристаллизации из водных растворов выделяются безводные галогениды рубидия и цезия ( в отличие от. [50]
Большой группой катализаторов алкилирования являются галогениды металлов, которые часто называют апротонными кислотами. Они обычно проявляют каталитическую активность в присутствии промоторов, с которыми образуют продукты кислотного характера. Из катализаторов этого типа чаще всего применяются следующие безводные галогениды [6, 18]: хлористый алюминий, бромистый алюминий, треххлористое железо, хлористый цинк, треххлористый титан и четыреххлористый титан. Сравнительно реже применяются для алкилирования четыреххлористое олово, четыреххлористый цирконий, пятихлористая сурьма, шестихлористый ванадий, двзгхлористая медь и другие галогениды. [51]
 |
Прибор для получения SiI4. [52] |
Восстановление галогенидов или сульфидов происходит с большим трудом, так как склонность водорода соединяться с хлором, бромом, иодом или серой меньше, чем с кислородом. В соответствии с возрастанием сродства к водороду ( HF, H2O, HC1, НВг, H2S, HI) лучше всего восстанавливаются фториды и значительно хуже хлориды. Однако применение галогенидов в большинстве случаев не имеет каких-либо преимуществ; как правило, безводные галогениды получаются из окислов лишь с большим трудом. Галогениды применяют только тогда, когда образование смешанной окисной фазы затрудняет полное восстановление. [53]
Промышленность броморганических соединений вырабатывает значительные количества гексабромбензола. Производство полибромированных соединений, замещенных в ароматическом кольце, требует повышенной температуры и длительного времени контакта. Обычно в качестве растворителя используют малолетучие соединения, такие как тетрахлорэтан, дибромэтан ( Заявка 1933486, ФРГ, 1971), а также проводят реакцию в присутствии олеума. В качестве катализаторов применяют железную пудру, безводные галогениды железа или их комбинации с иодом, или галогениды алюминия. [54]
Страницы: 1 2 3 4