Высшие галогениды
Cтраница 2
Летучесть ЭГ растет при увеличении п, что обусловливает диспропорцио-нирование низших ЭГ при нагревании. Это объясняет и тот факт, что некоторые высшие галогениды более стойки не в твердом, а газообразном состоянии. [17]
 |
Взаимосвязь между стандартными энтальпиями образования высших оксидов элементов IV и V групп. [18] |
Летучесть галогенидов ЭГ растет при увеличении числа л, что обусловливает способность к диспропорционированию низших галогенидов при нагревании. Это объясняет и тот факт, что некоторые высшие галогениды более стойки не а твердом, а газообразном состоянии. [19]
Фтор, как наиболее энергичный окислитель, способен образовывать высшие галогениды ЭГе, из которых CrFe - твердое вещество, MoFe - легкокипящая жидкость, a WFe - газ, что свидетельствует об увеличении тенденции к образованию молекулярных структур. Низшие фториды СгР2 и CrF3 еолеобразны и тугоплавки. У молибдена и особенно у вольфрама число известных фторидов значительно меньше. Ни один из фторидов Мо и W не является солеобразным. [20]
Фтор, как наиболее энергичный окислитель, способен образовывать высшие галогениды ЭГб, из которых CrFg - твердое вещество, MoFe - легкокипящая жидкость, a WFg - газ, что свидетельствует об увеличении тенденции к образованию молекулярных структур. Низшие фториды CrF2 и CrFg солеобразны и тугоплавки. У молибдена и особенно у вольфрама число известных фторидов значита ьно меньше. Ни один из фторидов Мо и W не является солеобразным. [21]
 |
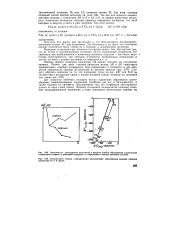
Зависимость стандартной энтальпии сублимации элементных веществ IV группы от порядкового номера элемента. [22] |
Полярность связей в соединениях с ростом w уменьшается: для w 1 и 2 связь близка к ионной, для w шмак она приближается к ковалентной. Поэтому, например, низшие оксиды-и гидроксиды являются основными, высшие - кислотными, многие низшие галогениды - ионные кристаллы ( хорошо растворимые соли), высшие галогениды - легкоплавкие, легкодетучие вещества, подвергающиеся гидролизу. [23]
Полярность связей в соединениях с ростом ш уменьшается: для w 1 и 2 связь близка к ионной, для w - ш акс она приближается к ковалентной. Поэтому, например, низшие оксиды и гидроксиды являются основными, высшие - кислотными, многие низшие галогениды - ионные кристаллы ( хорошо растворимые соли), высшие галогениды - легкоплавкие, легколетучие вещества, подвергающиеся гидролизу. [24]
Наиболее активным окислителем является марганец в высшей степени окисления. Химические связи, особенно в соединениях с высокими степенями окисления, имеют ковалентный характер. Высшие галогениды летучи и легко гидролизуются в водных растворах. [25]
 |
Некоторые физико-химические свойства высших галогенидов элементов Vffi-группы. [26] |
Из высших галогенидов получены в индивидуальном виде Сг. Все высшие галогениды синтезируют из простых веществ при избытке галогена. [27]
Полярность связей соединениях с ростом степени окисления уменьшается: для значений w 1 и 2 связь близка к ионной, для H HHUC она приближается к ковалентной. Поэтому, например, низшие оксиды и гидроксиды ( / - элементов проявляют основные свойства, высшие оксиды - кислотные свойства. Многие низшие галогениды - ионные кристаллы ( хорошо растворимые соли), высшие галогениды представляют собой легкоплавкие, легколетучие вещества, подвергающиеся гидролизу. [28]
Галогениды щелочных металлов ( за исключением, может быть, лития), щелочноземельных металлов ( кроме бериллия) и большинства лантанидов и нескольких галогенидов актинидов можно считать чисто ионными галогенидами. По мере увеличения отношения заряд / радиус, однако, ковалентность возрастает. Нечто подобное имеет место и для металлов с переменной степенью окисления; низшие галогениды в большей мере являются ионными, в то время как высшие галогениды - ковалентные соединения. В качестве примеров можно привести РЬС12 и РЬС14, а также UF4, который является ионным соединением, тогда как UF6 - газообразное ковалентное соединение. [29]
Галогениды щелочных металлов ( за исключением, может быть, лития), щелочноземельных металлов ( кроме бериллия) и большинства лантанидов и нескольких галогенидов актинидов можно считать чисто ионными галогенидами. По мере увеличения отношения заряд / радиус, однако, ковалентность возрастает. KCI - чисто ионное соединение, тогда как TiCl4 фактически ковалентное. Нечто подобное имеет место и для металлов с переменной степенью окисления; низшие галогениды в большей мере являются ионными, в то время как высшие галогениды - ковалентные соединения. В качестве примеров можно привести РЬС12 и РЬС14, а также UF4, который является ионным соединением, тогда как UFe - газообразное ковалентное соединение. [30]
Страницы: 1 2 3