Диполярный ион
Cтраница 1
Диполярные ионы не перемещаются в электрическом поле. При зна чениях рН среды ниже значения р [ катион а-аминокислоты ( аммониевая форма) движется к катоду; при phJ виши, чем pi, ацилат-ион а-аминокислоты перемещается к аноду. [1]
Диполярный ион аминокислоты можно рассматривать как молекулу, в которой карбоксильная группа имеет большое сродство к электрону, а аминная группа - к протону. Существует такое значение рН - так называемая изоэлектрическая точка pJ, - при котором аминокислота существует в максимальном количестве в виде диполярных, нейтральных молекул. [2]
Из диполярного иона, полученного нефотохимическим путем, образуется соединение ( 4), как и должно быть, если диполярный ной служит ннтермедиатом в фотохимической реакции. При дальнейшем изучении этого процесса был установлен другой аспект механизма реакции. [3]
Сорбция диполярных ионов представляет собой значительно более сложное явление, чем сорбция ионов, несущих один или одноименные заряды. Хорошо известно, что аминокислоты, полипептиды и белки, а также ряд других органических соединений, в некоторой области значений рН обладают одновременно ионизированными кислотными и основными группами. Взаимодействие такого ряда ионов с ионитами должно проявляться в сочетании электростатического притяжения и электростатического отталкивания. Сорбция аминокислот на сульфосмолах в Н - форме протекает без эквивалентного обмена с ионами водорода. [4]
Сорбция диполярных ионов катионитами в водородной форме приводит к превращению диполярного иона в катион и тем самым подавляется действие отрицательного заряда. [5]
Аминимиды представляют собой диполярные ионы, включающие положительно заряженный азот, связанный с азотом, несущим отрицательный заряд. [6]
При сорбции диполярных ионов должно наблюдаться, помимо электростатического притяжения, также электростатическое отталкивание. [7]
Емкость сорбции диполярного иона катионитом в водородной форме во много раз превышает сорбционную емкость того же катионита в солевой форме, так как при использовании солевой формы ионита не снимается второй заряд диполярного иона. [8]
Изложенные выше принципы сорбции диполярных ионов позволяют понижать обменную емкость смол, заметая часть ионов водорода на смоле ионами натрия, калия, аммония или другими ионами металлов. Именно на таких частично замещенных смолах или смолах в смешанной H - NH4 - форме и удалось произвести очистку альбомицияа. [9]
При pKipHpK2 аминокислота является диполярным ионом ( цвиттерионом), так как она заряжена одновременно двумя знаками. [10]
С другой стороны, разделение диполярных ионов и других типов ионов может быть осуществлено с большей эффективностью при использовании специфических сорбционных свойств диполярных ионов. [11]
Особый случай представляют аминокислоты, образующие диполярные ионы; они будут рассмотрены ниже в разделе, посвященном азот-углеродным соединениям. [12]
Поглощаемые по уравнению ( 1) диполярные ионы на сульфокатионитах в водородной форме превращаются, следовательно, в катионы. Процесс сорбции, представленный уравнением ( 2), определяется механизмом чистого ионного обмена. [13]
Первоначально образующийся аддукт разрушается и возникающий диполярный ион присоединяется по карбонильной группе кетона. [14]
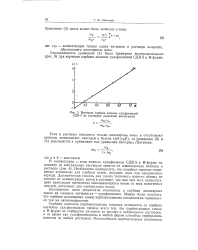 |
Изотерма сорбции аланина сульфосмолой. СДВ-3 из растворов различной кислотности. [15] |
Страницы: 1 2 3 4