Диполярный ион
Cтраница 4
Как и для эквивалентного ионного обмена, протекающего с участием ионов органических веществ, процесс непосредственной сорбции диполярных ионов, состоящий в превращении водородной формы резината в аминокислотную, сопровождается ростом энтропии системы. [46]
Таким образом, появляется возможность компенсировать изменение термодинамического потенциала гидролиза пептидной связи путем изменения термодинамического потенциала при сорбции диполярного иона. Наиболее вероятным представляется процесс синтеза из полипептидов среднего молекулярного веса, а также процессы диспропорционирования. [47]
Другой способ осуществления процесса сорбции ионов на карбоксильных катионитах в Н - форме состоит в использовании особенностей процесса сорбции диполярных ионов. Процесс сорбции дмнолярных ионов карбоксильными смолами в водородной форме был использован для выделения н очистки ряда веществ. Необходимо отметить, что этот процесс прямо противоположен процессу сорбции простых катионов иа карбоксильных смолах. Диполярные ионы сорбируются на карбоксильных смолах в Н - форме и не сорбируются на этих смолах и их солевых формах. Приведенная на рис. 11 кривая зависимости сорбпруемости антибиотика альбоми-цпна карбоксильной смолой КМТ от содержания ионов водорода в ионите показывает, что диполярные ионы альбомицина вступают в реакцию обмена только с теми ионогенными группами, которые находятся в Н - фор-ме. Если содержание ионов водорода в смоле меньше 2 мг-экв / г, то альбомицин совсем не сорбируется. Максимум на кривой сорбируемости связан с увеличением степени набухания ионита при переводе его в солевую форму. На карбоксильной же смоле в Na-форме альбомицин не сорбируется, несмотря на очень большую степень набухания смолы в этой форме. [48]
Возможно также, что некоторая часть ксантогената разлагается в результате реакции, при которой происходит образование промежуточного соединения типа диполярного иона [24], рассмотренного выше, из которого олефины могут образоваться по механизму, в значительной степени отличающемуся от согласованного механизма реакции Чугаева. [49]
Дальнейшее увеличение длины цепи в моноаминомонокарбо-новых соединениях приводит снова к усилению эффекта отталкивания вещества от ионообменной смолы, так как диполярный ион такого типа приобретает в растворе скрученную конформацию со сближенными функциональными группами. Так, со-аминоэнан-товая кислота уже плохо сорбируется солевой формой катионита. Вместе с тем повышение ионной силы раствора не вызывает увеличения сорбирусмости этой кислоты, в то время как увеличение количества ацетона в растворе приводит к понижению степени ионизации ш-аминоэнантовой кислоты, уменьшению эффекта электростатического отталкивания от катионитов и увеличению емкости сорбции катионитами в солевой форме. [50]
Дальнейшее увеличение длины цепи в моноаминомонокарбо-новых соединениях приводит снова к усилению эффекта отталкивания вещества от ионообменной смолы, так как диполярный ион такого типа приобретает в растворе скрученную конформацию со сближенными функциональными группами. Так, со-аминоэнан-товая кислота уже плохо сорбируется солевой формой катионита. Вместе с тем повышение ионной силы раствора не вызывает увеличения сорбируемости этой кислоты, в то время как увеличение количества ацетона в растворе приводит к понижению степени ионизации со-аминоэнантовой кислоты, уменьшению эффекта электростатического отталкивания от катионитов и увеличению емкости сорбции катионитами в солевой форме. [51]
Первую стадию, следовательно, составляет обратимое протони-рование атома азота, а вторая стадия заключается в нуклеофиль-ной атаке фосфат-аниона на атом фосфора диполярного иона. [52]
С другой стороны, разделение диполярных ионов и других типов ионов может быть осуществлено с большей эффективностью при использовании специфических сорбционных свойств диполярных ионов. [53]
Они показали, что электродный процесс в этой области характеризуется следующими промежуточными стадиями: диффузией анионов, рекомбинацией анионов с донорами протонов с образованием диполярных ионов, восстановлением диполярных ионов. Из кинетических токов найдены константы скорости рекомбинации и диссоциации никотиновой кислоты с участием иона гидроксо-ния. Показано, что эти константы близки к соответствующим константам для других пиридинкарбоновых кислот. [54]
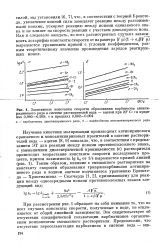 |
Зависимость константы скорости образования карбинолов антипиридинового ряда в системе растворителей вода - ацетон при 20 С.. в пределах 0 990 - 0 999. s в пределах 0 002 - 0 004. [55] |
Бренсте-да, увеличение ионной силы замедляет реакцию между разноименными ионами, ускоряет реакцию между ионами одинакового знака и не влияет на скорость реакции с участием диполярного иона. [56]
Один из способов преодоления трудностей в количественном изучении ионообменной сорбции аминокислот состоит во введении диссоциационных представлений, например в предположении о сорбции наряду с катионами аминокислот их диполярных ионов, что, естественно, должно зависеть от рН и не только внешнего раствора, но и гелевой фазы ионйта. Второй вариант подхода заключается в использовании представления об изменчивости коэффициента активности резинатов при изменении рН внешнего ( и внутреннего) раствора, причем эти изменения могут быть существенными. [57]
Для объяснения противоречащего кривым потенциометрического титрования факта малой сорбируемости катионов ( не только больших, но и малых размеров), а также и для объяснения причин сорбируемости диполярных ионов карбоксильными смолами в Н - форме достаточно предположить, что наиболее замедленным процессом в системе сорбцион-ных процессов является не диффузия сорбируемых ионов, а диффузия десорбируемых с карбоксильных смол ионов водорода. Действительно, в соответствии с кривыми потенциоМ етр Ического титрования ( рис. 5) равновесная концентрация ионов водорода в зерне смолы должна быть ничтожно малой. [58]
Они показали, что электродный процесс в этой области характеризуется следующими промежуточными стадиями: диффузией анионов, рекомбинацией анионов с донорами протонов с образованием диполярных ионов, восстановлением диполярных ионов. Из кинетических токов найдены константы скорости рекомбинации и диссоциации никотиновой кислоты с участием иона гидроксо-ния. Показано, что эти константы близки к соответствующим константам для других пиридинкарбоновых кислот. [59]
Страницы: 1 2 3 4