Галогенкетон
Cтраница 3
 |
Плоская диаграмма октантов. [31] |
Легко видеть, что аксиальное правило галогенкетонов ( рис. 14 - 38) представляет собой частный случай правила октантов с дополнительным условием, что влияние аксиального галогена, находящегося по соседству с карбонильной группой, перекрывает влияние всех остальных заместителей вследствие большой атомной рефракции хлора, брома и иода ( стр. [32]
Следующие методы позволяют получить единственный изомер галогенкетона при условии, что предшественники свободны от примесей изомеров и в процессе выделения также не происходит изомеризации. С-2 и легко деформилируются разбавленной щелочью. Очень гибкий метод использует енолборинаты. [33]
В табл. 151 - VIII приведены те галогенкетоны, из которых были получены продукты реакции Фаворского. Кроме того, в эти таблицы включены характерные примеры реакции Фаворского, когда не было получено положительных результатов. Галогенкетоны расположены в таблицах в следующем порядке: ациклические моногалогенкетоны, алициклические моногалогенкетоны ( за исключением стероидов), арилалкилмопогалогенке-тоны, стероидные моногалогенкетоны, дигалогенкетоны, тригало-геикетоны. Ввиду того что при галогенировании несимметричных кетонов могут образоваться изомеры с различным положением галогена, знак вопроса после обозначения положения галогена означает, что имеются сомнения в идентичности или чистоте указанной структуры. Выходы, приведенные в таблицах, даны для продуктов перегруппировки, за исключением тех случаев, когда число заключено в скобки. В этом случае данные относятся к выходу свободной кислоты, полученной из первичного продукта перегруппировки. [34]
Весьма своеобразно поведение при различных реакциях - галогенкетонов - соединений, содержащих у одного и того же углеродного атома весьма реакционноспособную карбонильную группу и очень подвижный атом галогена. [35]
Примером могут служить а-галогензамещенные циклогексаноны, в случае которых аксиальный галогенкетон проявляет поглощение при более низкой частоте, чем соответствующее ему экваториальное соединение. [36]
Таким образом, А. Е. Фаворским была обнаружена способность ct - галогенкетонов вступать в различные реакции и своеобразное поведение их при взаимодействии с некоторыми реагентами. [37]
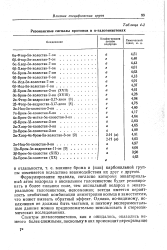 |
Резонансные сигналы протонов в а-галогенкетонах. [38] |
Формулирование правила, согласно которому экваториальный атом водорода в аксиальном галогенкетоне будет резонировать в более сильном поле, чем аксиальный водород в экваториальном галогенкетоне, невозможно; всегда имеется вероятность необычной комбинации анизотропии кольца и заместителя, что может вызвать обратный эффект. Однако, по-видимому, исключения не должны быть частыми, и поэтому экспериментальные данные можно предположительно использовать в стереохи-мических исследованиях. [39]
Ранее уже упоминалось, что определение конфигурации на основе правила галогенкетонов может оказаться неправильным, если кетонный цикл существует в форме ванны. Формы ванны не настолько маловероятны, как может показаться, поскольку установлено [26], что разница в энергиях форм кресла и ванны для циклогексанона составляет лишь половину ( 2 7 по сравнению с 5 6 ккал / моль) соответствующей разницы для циклогексана. Вследствие этого неблагоприятные конформационные взаимодействия в замещенном цикло-гексаноне могут легко заставить такую молекулу принять конформацию ванны ( ср. [40]
Если с протоном координируется атом углерода, около которого в исходном галогенкетоне был галоген, получается кислота, изомерная той, которая должна была бы образоваться по схеме Фаворского. [41]
Тиазолы могут быть легко получены синтезом Ганча ( нз тио-амида и галогенкетона), а их восстановление в тиазолидины проходит очень легко. Гидролиз тиазолидинов также осуществляется без труда и дает р-аминоалкантиолы. Таким образом, конечным итогом этой цепи превращений является синтез р-аминоалкантио-лов из тиоамидов, которые используются как источник азота и серы. Завершающим этапом в этом варианте синтеза р-аминоал-килсульфидов является превращение тиола в сульфид. [42]
В настоящее время известно, что а-галогенкетоны могут превращаться в изомерные а - галогенкетоны. [43]
Весьма вероятно, что механизм превращения оксиальдегидов в кислоты аналогичен кислотному превращению галогенальдегидов и галогенкетонов. Неспособность а-оксиальдегидов со вторичной спиртовой группой к кислотному превращению объясняется меньшей подвижностью гидроксила при вторичном углеродном атоме по сравнению с гидроксилом при третичном углероде. [44]
Весьма вероятно, что механизм превращения оксиальдегидов; кислоты аналогичен кислотному превращению галогенальдегидов 1 галогенкетонов. Неспособность а-оксиальдегидов со вторичной: пиртовой группой к кислотному превращению объясняется мень-ней подвижностью гидроксила при вторичном углеродном атоме по сравнению с гидроксилом при третичном углероде. [45]
Страницы: 1 2 3 4