Другой галогеноводород
Cтраница 2
Необходимо отметить, что температуры плавления и кипения HF аномально высоки по сравнению с другими галогеноводородами. Причина этого необычного поведения заключается в наличии сильной водородной связи между молекулами HF в жидком состоянии, что уже обсуждалось в разд. Поскольку молекула HF имеет небольшой размер и способна образовывать сильные водородные связи, HF очень хорошо смешивается с водой. Но и другие галогеноводороды, хотя и не способны к образованию прочных водородных связей, тоже хорошо растворимы в воде. Как отмечалось в разд. [16]
Таким образом, прочность связи Н - F - главная причина того, почему это вещество является в водном растворе значительно более слабой кислотой, нежели другие галогеноводороды. [17]
Как отмечалось ранее, при растворении галогеноводородов в воде происходит их диссоциация на ионы и образуются водные растворы соответствующих галогено-водородных кислот. В отличие от других галогеноводородов фтористый водород диссоциирует в воде слабо, в связи с этим образующаяся фтористоводородная кислота является слабой, эта кислота лишь немного сильнее уксусной. Такое аномальное поведение фтористого водорода объясняется ассоциацией молекул фтористого водорода вследствие возникновения между ними водородных связей ( см. § 7, гл. HF на ионы требуется дополнительная затрата энергии на разрыв водородных связей. [18]
Следует подчеркнуть, что обращение нормальной ориентации присоединения под влиянием перекисей имеет место только в случае НВг. Иначе обстоит дело в реакциях присоединения других галогеноводородов. В случае HF для образования радикала F требуется слишком большое количество энергии во второй стадии, а в случае присоединения HI, хотя радикал Ь образуется и легко, однако он недостаточно реакционноспособен для того, чтобы развить цепную реакцию. [19]
Для фтороводорода характерно образование устойчивых фторгидрогенатов. Известно много устойчивых кислых солей фтороводорода, в то время как другие галогеноводороды вообще не дают кислых солей. [20]
При этом частично разрываются водородные связи, так что диссоциация HF на ионы требует значительной затраты энергии. Поэтому фтороводород диссоциирует в водных растворах в значительно меньшей степени, чем другие галогеноводороды; константа диссоциации фтороводорода равна 7 - Ю 4, так что по силе эта кислота лишь ненамного превосходит уксусную. [21]
При этом частично разрываются водородные связи, так что диссоциация HF на ионы требует значительной затраты энергии. Поэтому фтороводород диссоциирует в водных растворах в значительно меньшей степени, чем другие галогеноводороды; константа диссоциации фтороводорода равна 7 - 10 - 4, так что по силе эта кислота лишь ненамного превосходит уксусную. [22]
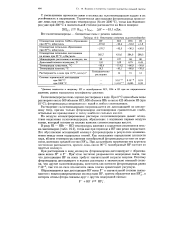 |
Некоторые свойства галогеноводородов. [23] |
При этом частично разрываются водородные связи, так что диссоциация HF на ионы требует значительной затраты энергии. Поэтому фтороводород диссоциирует в водных растворах в значительно меньшей степени, чем другие галогеноводороды, константа кислотности фтороводорода равна 7 - 10 4, так что по силе эта кислота лишь слегка превосходит уксусную. [24]
При этом частично разрываются водородные связи, так что диссоциация HF на ионы требует значительной затраты энергии. Поэтому фтороводород диссоциирует в водных растворах в значительно меньшей степени, чем другие галогеноводороды константа диссоциации фтороводорода равна 7 - 10 - 4, так что по силе эта кислота лишь ненамного превосходит уксусную. [25]
Связь водорода с фтором Н - F характеризуется очень высокой полярностью, что обусловливает резко выраженную склонность HF к ассоциации - образованию водородных связей ( см. гл. Этим объясняется то, что фтористый водород по свойствам значительно отличается от других галогеноводородов. [26]
 |
Физические свойства элементов главной подгруппы VI группы. [27] |
Меньшая активность плавиковой кислоты связана с образованием ассоциированных молекул H2F2 за счет водородных связей. Однако в некоторых случаях плавиковая кислота вступает в реакции, не характерные для других галогеноводородов. [28]
 |
Физические свойства элементов главной подгруппы VI группы. [29] |
Меньшая активность плавиковой кислоты связана с образованием ассоциированных молекул H Fa за счет водородных связей. Однако в некоторых случаях плавиковая кислота вступает в реакции, не характерные для других галогеноводородов. [30]
Страницы: 1 2 3