Гидрокарбонатный ион
Cтраница 2
Наибольшее увеличение концентрации ( мг / 100 г) от 9 1 до 146 4 ( среднее 35) происходит для гидрокарбонатного иона. [16]
В ( случае, если общая жесткость воды меньше 1 мг-зкв, расчет постоянной жесткости не производится, так как скорость распада гидрокарбонатного иона будет очень мала. Расчет не производится и при Са0 и Mgo больше 3 мг-экв, а также три р, 0 02, так как при столь большой жесткости и минерализации воды последняя не может иметь технического применения. [17]
Опыт многолетних наблюдений и специальных исследований обычных питьевых вод подсказывал, что их хорошие органолептические свойства в значительной мере зависят от содержания гидрокарбонатных ионов, поэтому гидрокарбонатные воды предпочтительнее в качестве питьевых, чем сульфатные и хлоридные. [18]
Однако подземные воды, производные от океанической воды, имеют другую общую минерализацию, и в составе их после натрия обычно стоит кальций, а после хлора часто гидрокарбонатный ион. Что касается сульфатов, то в некоторых водах они почти исчезают и взамен их появляется сероводород. Эти изменения объясняются процессами десульфатизации, доломитизации и обмена катионов. [19]
Обобщая фактический материал по изменению состава попутной воды нефтяных месторождений и результаты лабораторного изучения процессов смешения природных пластовых вод с водами, используемыми для закачки, можно сказать, что наиболее близки к прямолинейным зависимости содержания ионов хлора и натрия; существенно отклоняются от прямолинейных зависимости содержания гидрокарбонатных ионов и кальция, в меньшей степени - сульфатных ионов и магния. Поэтому определение доли смешивающихся вод по составу воды-смеси, которой является попутная вода, можно производить на основе теоретических прямолинейных диаграмм смешения, используя в качестве индикаторов ионы хлора и натрия, микрокомпоненты и общую минерализацию. [20]
Метод основан ва том, что для вод с рН более 8 3 при титровании пробы исследуемой воды кислотой в присутствии индикатора фенолфталеина, дающего переход окраски от красного к бесцветному, протекают реакции между сильной кислотой, гидроксиль-ными и карбонатными ионами, а в интервале рН от 8 3 до 4 5 ( ог перехода окраски фенолфталеина до перехода окраски метилового оранжевого) - с гидрокарбонатными ионами. [21]
Внесение минеральных удобрений может быть эффективно в следующих случаях. Содержание гидрокарбонатных ионов ( НСОз), то есть щелочность более 3 мг-экв / л, в этом случае известкование излишне. Величина прозрачности по диску Секки не превышает 50 см: если прозрачность составляет менее 50 см, удобрять пруд нецелесообразно. [22]
Соответствующий ему рациональный состав искусственной морской воды готовился по следующему рецепту: 26 3 г / л NaCl, 3 8 г / л MgSO4, 1 7 г / л MgCb, 1 25 г / л Na2SO4, 1 0 г / л СаС12, 0 90 г / л K2SO4, 0 14 г / л КВг. Содержание гидрокарбонатного иона НСОз - в морской воде довольно постоянно и составляет 0 1 г / л, тогда как содержание солей изменяется в различных водоемах, хотя их соотношение остается постоянным. [23]
Последнее уравнение показывает, что гидрокарбонатные ионы могут находиться в растворе только в том случае, когда в нем находится свободная углекислота. Итак, концентрация гидрокарбонатных ионов находится в функциональной зависимости от концентрации свободной углекислоты. [24]
При просачивании воды через почвы происходит окисление органики, в результате чего изменяется газовый состав воды: содержание кислорода уменьшается, а диоксида углерода увеличивается. Выделяющийся СО2 служит дополнительным источником образования гидрокарбонатного иона. [25]
Сравнивая концентрации ионов хлора и сульфата в воде Волги и Москвы-реки, легко убедиться в большей агрессивности воды Волги. Кроме того, в волжской воде меньше гидрокарбонатных ионов ( 73 мг / л), чем в воде Москвы-реки ( до 250 мг / л НСО-Г) Последнее свидетельствует о меньшей способности волжской воды образовывать на поверхности металла гидроокисно-карбонатные пленки, обладающие защитными свойствами. Вывод о большей агрессивности волжской воды, поступающей в г. Москву, по сравнению с водой Москвы-реки, подтверждается результатами наблюдений за коррозией гидротехнических сооружений на Москве-реке и канале им. [26]
Избыточное количество свободной углекислоты, действуя на углекислый кальций, превращает его в гидрокарбонат. Вследствие этой реакции увеличивается количество первоначально находящегося в растворе гидрокарбонатного иона, следовательно, концентрация равновесной углекислоты также должна быть повышена, чтобы удержать в растворе новое количество гидрокарбонатного иона. [27]
Общая щелочность воды определяет ее буфферные свойства при обработке кислыми реагентами. При этом в реакции участвуют в основном присутствующие в воде гидрокарбонатные ионы ( рНВоды8 4), реже - карбонатные и гидроксиль-ные ионы, а также гуматы. [28]
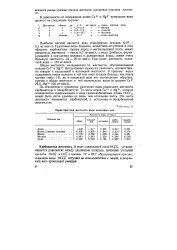 |
Характеристика жесткости воды некоторых рек. [29] |
По отношению к процессам умягчения воды различают жесткость карбонатную и некарбонатную. Та часть ионов Са2 и Mg2, которая эквивалентна содержащимся в воде гидрокарбонатным ионам НСО-3, может быть легче удалена из воды, чем остальная часть. Эта часть жесткости называется карбонатной, а остальная - некарбонатной жесткостью. [30]
Страницы: 1 2 3 4