Гаммафос
Cтраница 1
 |
Содержание 35S в крови и плазме собак после внутримышечного введения гаммафоса, меченного 35S, в дозе 50 мг / кг ( в процентах от введенного количества [ Ильин и соавт., 1976 ]. [1] |
Гаммафос, растворенный в воде и введенный парентерально, всасывается довольно быстро. [2]
 |
Гаммафос, разведенный в изотоническом растворе хлорида натрия, через 6 ч после внутримышечной инъекции. интерстициаль-ный отек, гранулоцитарная клеточная реакция ( Х120. [3] |
Внутримышечно введенный гаммафос эффективен у крыс, начиная с дозы 150 мг / кг. [4]
В случае гаммафоса были выявлены различия в защите нормальных и опухолевых тканей. Различия как в его распределении, так и метаболизме в тех и других тканях будут описаны в разделе, посвященном радиозащитному действию гаммафоса. [5]
Де-фосфорилированные молекулы гаммафоса обеспечивают защиту тем же способом, что и другие аминотиолы. В ряде дальнейших обменных превращений образуются молекулы меркаптоэтиламина ( цистеамина) и меркаптопропилами-на, деструкция и выведение которых происходит аналогичными описанными выше способами. [6]
Защитные дозы цистамина и гаммафоса, выраженные в виде одинакового процента от их среднелетальных доз, обеспечивают мышам неодинаковую защиту от летального воздействия ионизирующего излучения. У крыс эти различия, хотя они и меньше выражены, были все же в пользу гаммафоса. [7]
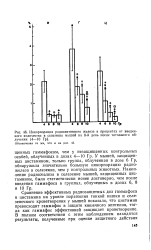 |
Инкорпорация радиоактивного железа в процентах от введенного количества в селезенке мышей на 8 - й день после тотального облучения ( 4 - 10 Гр. Обозначения те же, что и на 45. [8] |
Сравнение эффективных радиозащитных доз гаммафоса и цистамина на уровне поражения тонкой кишки и селезеночного кроветворения у мышей показало, что цистамин превосходит гаммафос в защите кишечного эпителия, тогда как гаммафос эффективней защищает кроветворение. [9]
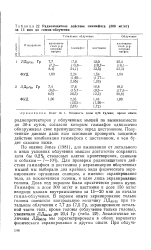 |
Радиозащитное действие гаммафоса ( 300 мг / кг за 15 мин до гамма-облучения. [10] |
Для проверки радиозащитного действия гаммафоса и цистамина у неравномерно облученных мышей мы выбирали два крайни вида физического экранирования организма свинцом, а именно: экранирование тела, за исключением головы, и одно лишь экранирование головы. Доза под экраном была практически равна нулю. Гаммафос в дозе 300 мг / кг и цистамин в дозе 150 мг / кг вводили мышам внутримышечно за 15 - 20 мин до начала гамма-облучения. [11]
Мы установили также, что гаммафос значительно повышает радиорезистентность крыс в интервале с 10 - й по 60 - ю минуту между его введением и началом облучения. Цистамин способен защищать крыс от летального действия излучений от 10 до 45 мин, как правило, с более низким ФУД, чем гаммафос. [12]
Большое значение в защитном действии гаммафоса придают напряжению кислорода в клетках. Было многократно показано, что защита кожи гаммафосом более выражена, если мыши вдыхают воздух, а не кислород. Радиосенсибилизатор гипоксических клеток мизо-нидазол, вводимый в комбинации с гаммафосом, приводит к снижению его защитного действия в коже и опухолях. Аналогично этому, сенсибилизирующее действие мизони-дазола ослабевает в присутствии гаммафоса. Результаты дают основания предполагать, что оба вещества действуют на одном уровне радиационного поражения. Кроме того, они демонстрируют, что гаммафос проникает в гипокси-ческие клетки опухоли. [13]
По нашим данным, внутримышечная инъекция гаммафоса ( 100 мг / кг), разделенная на 2 инъекции с общим объемом 1 мл / кг, вызывает рвоту у 80 % собак до 10 - й минуты после инъекции. Эффективным противорвотным препаратом и в случае гаммафоса является метоклопра-мид, вводимый внутримышечно в дозе 0 5 мг / кг. [14]
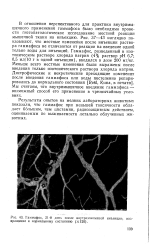 |
Гаммафос, 21 - й день после внутримышечной инъекции. возвращение к нормальному состоянию ( Х120. [15] |
Страницы: 1 2 3 4 5