Гаммафос
Cтраница 3
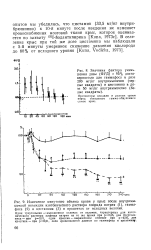
Экономические затруднения с опытами на средних и крупных лабораторных животных позволили нам лишь в ограниченном объеме сравнивать радиозащитное действие гаммафоса и цистамина у кроликов и собак по выживаемости до 45 - х суток после тотального гамма-облучения. Цистамин ( 70 мг / кг внутримышечно) постоянно обнаруживал у кроликов меньший защитный эффект, а в одном опыте ( см. рис. 48) практически совсем не дал эффекта. [31]
Анализ обмена сахаридов у крыс после введения исследованных радиопротекторов и физической нагрузки показал, что только у животных, получавших гаммафос, не имелось признаков нарушения их обмена. [32]
Сравнение эффективных радиозащитных доз гаммафоса и цистамина на уровне поражения тонкой кишки и селезеночного кроветворения у мышей показало, что цистамин превосходит гаммафос в защите кишечного эпителия, тогда как гаммафос эффективней защищает кроветворение. [33]
Yuhas ( 1980a) обнаружил также, что нормальная здоровая ткань активно накапливает протектор по сравнению с обычным градиентом, тогда как клетки солидной опухоли лишь пассивно поглощают гаммафос с довольно малой скоростью. Не было подтверждено первоначальное представление о нарушении дефосфорилирования гаммафоса в клетках опухоли. [34]
Сравнение эффективных радиозащитных доз гаммафоса и цистамина на уровне поражения тонкой кишки и селезеночного кроветворения у мышей показало, что цистамин превосходит гаммафос в защите кишечного эпителия, тогда как гаммафос эффективней защищает кроветворение. [35]
Только в первой серии опытов, проведенных в июле и августе, каждая комбинация гаммафоса ( 300 мг / кг) с увеличением дозы цистамина ( 30, 50 и 100 мг / кг) была значительно эффективней, чем один гаммафос. [36]
В наших опытах мы получили доказательство несомненной эффективности обоих веществ и после внутримышечного их введения, а если учесть менее выраженные местные изменения, обнаруженные у крыс и собак ( у собак косвенно - по биохимической реакции), то по сравнению с цистами-ном мы считаем гаммафос перспективным средством для массового применения. [37]
Один треугольник - выраженное отличие от величин, характерных для изотонического раствора хлорида натрия на то же время при р0 05, два треугольника - при р0 01, один крестик - выраженное отличие при р - 0 05, два крестика - при р0 01, если сравниваются данные по гаммафосу и цистамину. [39]
В отношении перспективного для практики внутримышечного применения гаммафоса было необходимо провести гистопатологическое исследование местной реакции мышечной ткани на инъекцию. Гаммафос, разведенный в изотоническом растворе хлорида натрия ( 4 % раствор рН 6 7; 0 5 мл / 10 г в одной инъекции), вводился в дозе 200 мг / кг. Меньше всего местные изменения были выражены после введения только изотонического раствора хлорида натрия. Мы считаем, что внутримышечное введение гаммафоса - возможный способ его применения в чрезвычайных условиях. [40]
Степень поражения тонкой кишки, точнее ее отрезка длиной 10 см, примыкающего к пилорической части желудка, оценивали по уменьшению ее массы на 3 - й сутки после облучения в дозах 7 - 16 Гр. Гаммафос существенно увеличивал массу отрезка кишки у мышей, облученных более низкими дозами - 8 и 10 Гр, а цистамин - у мышей, облученных более высокими дозами - 10 и 14 Гр. Никакого протективного действия на кишку не оказали радиозащитные вещества при облучении мышей в самой большой из использованных доз - 16 Гр. У мышей, облученных в дозе 14 Гр, гаммафос обнаружил намного меньшее защитное действие на исследуемый отрезок кишки, нежели цистамин. [41]
LAF [ гаммафос в дозе 600 мг / кг за 30 мин до введения цитотоксических веществ. Использованная доза составляет 2 / з величины ЛДбо гаммафоса у этой линии мышей. Гаммафос обеспечивал хорошую защиту стволовых клеток кроветворения от цитотоксического действия циклофосфа-мида, цис-платины и других веществ. [42]
АН СССР внутрибрюшинно вводили гаммафос мышам в дозах 300, 400 и 500 мг / кг за 15 мин до тотального рентгеновского облучения. [43]
При испытании комбинации протекторов гаммафос и цистамин разводили в общем растворе. Все растворы, в том числе и изотонический раствор хлорида натрия, контрольным мышам вводили внутримышечно в постоянном объеме ( 0 1 мл на 10 г массы тела), разделенном на две инъекции в обе икроножные мышцы. [44]
По нашим данным, внутримышечная инъекция гаммафоса ( 100 мг / кг), разделенная на 2 инъекции с общим объемом 1 мл / кг, вызывает рвоту у 80 % собак до 10 - й минуты после инъекции. Эффективным противорвотным препаратом и в случае гаммафоса является метоклопра-мид, вводимый внутримышечно в дозе 0 5 мг / кг. [45]
Страницы: 1 2 3 4 5