Гамметта
Cтраница 1
 |
Некоторые примеры за. [1] |
Гамметта, выведенное им в 1937 г. [1, 2] и проверенное тогда на примере 52 различных реакций ароматических соединений. В нем 0 приобрела характер универсальной константы, характерной для заместителя в бензольном кольце и сохраняющей постоянство в разнообразных реакциях, ар - константы реакции, независимой от природы заместителей и варьирующей в зависимости от типа реакции, условий среды и других внешних по отношению к органической молекуле факторов. [2]
Гамметта возможно в том случае, когда известен механизм реакции, и выводят формулу для расчета с учетом всех стадий ( см. стр. Если применять уравнение Гамметта-Тафта IK этой реакции - в целом, то, как показали те же авторы, при концентрации серной кислоты 35 и 40 % реакция не подчиняется уравнению Гамметта. Гамметта и значение р положительно. Это безусловно не случайное Совпадение, которое трудно ожидать для четырех членов серии, а вполне закономерное явление: заместители в ионах триарилкарбония влияют на склонность иона карбония к отрыву гидрид-иона от изопропилового спирта, протонированного при данной концентрации серной кислотой определенным образом. Противоречивые значения р, полученные для разных серий в различных условиях, говорят скорее всего о том, что ( реакция окисления хромовой кислотой состоит из нескольких стадий, значение которых для реакции может изменяться. [3]
 |
Скорость олигомеризации пропилена по областям кислотности сульфата никеля. [4] |
Гамметта: Igk lg а - - аН0, где k - константа скорости катализируемой реакции; Я0 - функция кислотности Гамметта; а и а - эмпирические константы для каждого типа реакции. Кв - обратный логарифм константы протонизации эталонного индикатора в разбавленном растворе, а ВН / В0 - экспериментально определяемое ( в случае твердых кислот - по окраске) отношение протонированной и депротонированной форм индикатора. Существенное отличие каталитических реакций с твердыми кислотами и основаниями от таковых в растворах заключается в следующем. Однако при сложных многостадийных и параллельно-последовательных реакциях образование промежуточного целевого продукта не будет пропорционально суммарной кислотности поверхности, что обусловливается разными значениями констант а и а каждой из стадийных реакций. В результате активность катализатора по целевому продукту будет пропорциональна концентрации активных центров некоторой оптимальной кислотности, как это, например, следует ( рис. I.10) для реакции олигомеризации пропилена. Аналогичного типа зависимость наблюдается для гидролитического разложения 4 4-диметилдиоксана - 1 3 в изопрен на фосфатных катализаторах. [5]
Гамметта хорошо соблюдается только в том случае, если таутомерное равновесие смещено в сторону одной из форм. Если же обе формы присутствуют в равновесии в заметных количествах, то наблюдаются отклонения от линейной зависимости. [6]
 |
Графическое изображение уравнения Гамметта. [7] |
Гамметта дает не всегда и не для всех заместителей хорошие результаты. [8]
Гамметта, справедливое при условии аддитивности констант ( Jaffe, 1953): Мы не будем останавливаться на детальном анализе этих результатов, так как недостаток данных не позволяет установить границы применимости изложенного метода. Однако следует указать, что полученное на рис. 10 линейное соотношение, несмотря на неприменимость обычного уравнения Гамметта к реакциям деацилирования ( ап-ко 2 ( а0) - - 3 2; Кто ], Verkade, Wepster, неопубликов. С другой стороны, различия в углах поворота ср, вычисленных для соответственно замещенных нитробензолов и я-нитроанилинов на основании спектральных данных ( стр. Наблюдаемая, несмотря на это, линейность может быть, вероятно, обусловлена взаимной компенсацией эффектов различий мезомерного взаимодействия и ван-дер-ваальсового отталкивания ( ср. [9]
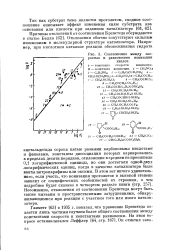 |
Соотношение между скоростью и равновесием ионизации кислот. [10] |
Гамметт [63] в 1935 г. показал, что уравнение Бренстеда является лишь частным случаем более общего соотношения между константами скорости и константами равновесия. [11]
Гамметту определяется силой основания, способного ионизировать в испытуемом растворе кислоты, и степенью его ионизации. Она равна отношению концентраций ионизированной и неионизированной форм индикатора СБН В. [12]
Трактовка Гамметта упрощает ситуацию, рассматривая влияние, заместителей, находящихся только в тех положениях, при которых влияние пространственных факторов отсутствует. Мета-заместитель изменяет скорость реакции или смещает равновесие только в результате индукционного влияния. Действие пара-заместителя является результатом наложения резонансного и индукционного эффектов, причем либо тот. Если значения ст определены для разных заместителей в одной какой-нибудь реакции, то эти значения могут быть использованы для определения константы р и для других реакций. Измеряют константы скорости или равновесия и строят кривую зависимости логарифмов этих констант от значений а. [13]
Трактовка Гамметта упрощает ситуацию, рассматривая влияние заместителей, находящихся только в тех положениях, при которых влияние пространственных факторов отсутствует. Мета-заместитель изменяет скорость реакции или смещает равновесие только в результате индукционного влияния. Действие пара-заместителя является результатом наложения резонансного и индукционного эффектов, причем либо тот, либо другой могут иметь доминирующее значение ( ср. Если значения а определены для разных заместителей в одной какой-нибудь реакции, то эти значения могут быть использованы для определения константы р и для других реакций. Измеряют константы скорости или равновесия и строят кривую зависимости логарифмов этих констант от значений а. [14]
Уравнение Гамметта прошло широкую экспериментальную проверку и подтверждено для очень большого числа примеров. В обзоре Жаффе [3] указывается 400 реакций, к которым хорошо применимо уравнение Гамметта. За последующие 6 лет это число еще значительно возросло. [15]
Страницы: 1 2 3 4