Коагулирующий ион
Cтраница 3
Пептизация происходит вследствие удаления из осадка коагулирующих ионов ( при промывке) или в результате адсорбции пепти-затора ( специального вещества) коллоидными частицами осадка. [31]
Согласно теории ДЛФО, критическая концентрация коагулирующего иона не должна зависеть от размера коллоидной частицы, но Визе и Хили [279] показали, что при дальнейшем уточнении теории, принимая во внимание и первый, и второй минимумы, можно объяснить, что устойчивость коллоидной системы возрастает с увеличением размера частиц. Стабильность достигает максимума, а затем убывает. [32]
Очевидно, что чем больше валентность коагулирующих ионов, тем сильнее они сжимают диффузный слой противоионов. Однако механизм коагулирующего действия электролитов не сводится только к сжатию диффузного слоя. [33]
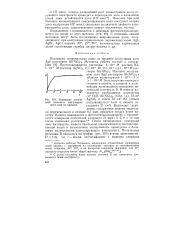 |
Изменение оптиче - AgNO3 и затем 10 см3 KJ ( объем ской плотности коагулирую - получающегося золя в кювете со-щего золя во времени. ставляет 21 см3. Включают секун. [34] |
Наконец, при еще больших концентрациях коагулирующего иона наступает вторая зона коагуляции ( IV зона), связанная со сжатием двойного электрического слоя, существующего вокруг коллоидных частиц. [35]
При коагуляции коллоидов обычно происходит адсорбция коагулирующих ионов коллоидными частицами, которая вызывает изменения в структуре двойного электрического слоя в растворе, направленные в сторону уменьшения его диффузной части. [36]
Ск обратно пропорционально шестой степени валентности коагулирующего иона. Эту же зависимость отражает экспериментально найденное правило Шульце - Гарди. Полученное отличное совпадение хорошо подтверждает правильность теории коагуляции лиофобных золей. [37]
Происходит это потому, что поглощенные осадком коагулирующие ионы при промывании его водой будут постепенно переходить в раствор. [38]
 |
Чередование зон устойчивости. [39] |
Чередование зон устойчивости характерно для электролитов, коагулирующие ионы которых - поливалентные ионы Fe8, Тп4 Сг3 и органические ионы. Как видно на рисунке, уменьшение абсолютной величины заряда частицы совпадает с первой областью коагуляции. [40]
 |
Чередование зон устойчивости. [41] |
Чередование зон устойчивости характерно для электролитов, коагулирующие ионы которых многозарядные ионы Fe3, Th 1 1 -, Сг3 и органические ионы. Как видно на рисунке, уменьшение абсолютной величины заряда частицы совпадает с первой областью коагуляции. Затем частица вновь приобретает заряд, но уже противоположного знака, чему соответствует вторая область устойчивости. Дальнейшее повышение концентрации приводит к падению абсолютной величины заряда частицы и к коагуляции золя. Сравнение устойчивости и заряда показывает, что явление неправильных рядов вызвано перезарядкой поверхности. [42]
Правило Шульце позволяет решить вопрос о валентности коагулирующих ионов. [43]
Высокая степень коагуляции глинистых растворов обусловлена влиянием коагулирующих ионов. В соответствии с воззрениями коллоидной химии коагулирующими ионами ( противо-ионами) для глинистых частиц, заряженных, как правило, отрицательно, являются ионы металлов. Обычно в природе для глинистых частиц коагулирующими являются ионы натрия, калия, магния, кальция. При этом интенсивность коагулирующего воздействия возрастает с увеличением валентности катиона. Анионы, связанные с коагулирующими катионами, также влияют на коагуляцию. Так, наиболее сильное коагулирующее действие на глинистые частицы оказывает хлористый натрий; менее активен сернокислый натрий. [44]
Порог коагуляции данного коллоида зависит от валентности коагулирующего иона. [45]
Страницы: 1 2 3 4