Коагулирующий ион
Cтраница 4
При удалении цветности с использованием в качестве коагулирующих ионов Fe2 и F3 возникает ряд особенностей. [46]
Порог коагуляции данного коллоида зависит от валентности коагулирующего иона. [47]
Причинами пептизации являются либо удаление из осадка коагулирующих ионов, либо образование двойных электрических слоев или сольватных оболочек у коллоидных частиц вследствие адсорбции ими ионов пептизатора. [48]
Пептизация может происходить вследствие удаления из раствора коагулирующих ионов, вызывающих укрупнение части, или адсорбции пептизатора, сопровождающейся образованием двойного электрического слоя и возникновением сольватнои оболочки на коллоидных частицах. Во всех случаях частицы разобщаются между собой и вследствие теплового движения распределяются по всему объему дисперсионной среды. [49]
 |
Коагулирующие концентрации некоторых электролитов ( ммоль / л для коллоидного раствора сернистого мышьяка ( 7 54 ммоль As2S3 в 1 л. [50] |
Порог коагуляции данного коллоида зависит от валентности коагулирующего иона. [51]
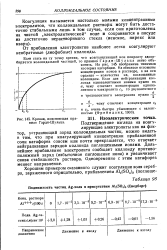 |
Кривая, поясняющая пра - 311. ИзОЭЛектрИЧССКая ТОЧКа.| Подвижность частиц Ag-золя в присутствии A12 ( SO4 3 ( Сведберг. [52] |
Если стать на ту точку зрения, что коагулирующий ион попросту адсорбируется коллоидальной частицей, то правило Гарди-Шульца легко объяснить. На рис. 145 изображена типичная изотерма адсорбции. На абсциссе отложены концентрации ионов в растворе, а на оси ординат - количества их, поглощенные коллоидом. Если для нейтрализации коллоида одновалентными ионами нужно их. [53]
Согласно правилу Шульце-Гарди, при коагуляции золя электролитами коагулирующий ион всегда имеет заряд, противоположный заряду коллоидной частицы; порог коагуляции при этом тем меньше, чем выше валентность коагулирующего иона. Так, отрицательно заряженные золи золота и As2S3 коагулируют под влиянием катиона; положительно заряженные золи, подобно Fe ( OH) 3, коагулируют под. [54]
На коагуляцию золей влияет также и степень гидратации коагулирующих ионов. [55]
Страницы: 1 2 3 4