Гашение - флуоресценция
Cтраница 2
Исследование гашения флуоресценции электронно-возбужденных частиц различными газами позволяет установить некоторые общие закономерности, характеризующие переходы энергии электронного возбуждения частиц в различные формы энергии соударяющихся частиц. [16]
Для резонансного гашения флуоресценции органических веществ примесями, как показали С. И. Вавилов и Галанин81, необходимо соблюдение двух условий: 1) чтобы спектр флуоресценции люминесцирующего вещества накладывался на спектр поглощения гасителя; 2) чтобы молекула гасителя сама не обладала флуоресцентной способностью. Первое условие необходимо для установления резонанса, второе - для рассеивания гасителем воспринятой энергии. При резонансном гашении нельзя говорить о поглощении гасителем квантов света излученных флуоресцирующим веществом, подобно поглощению света светофильтром ( внутренний светофильтр), так как концентрация гасителя обычно бывает чрезвычайно малой. [17]
Относительно причины гашения флуоресценции флуорексона в щелочной среде и изменения флуоресценции в присутствии катионов существуют различные мнения. [18]
При исследовании472 478 гашения флуоресценции урана во фториде натрия некоторыми элементами установлено, что помехи флуоресценции зависят от соотношения концентраций и примесей урана. [19]
Все разобранные случаи гашения флуоресценции посторонними веществами не сопровождаются изменением свойств люмине-сцирующей молекулы. [20]
Уже отмененный эффект гашения флуоресценции 2 - ( о-оксифе-нил) - бензоксазола в присутствии меди ( см. стр. Было показано, что 2 - ( о-оксифенил) - бензоксазол в кислой, нейтральной и слабощелочной средах флуоресцирует зеленым цветом, а в сильнощелочной-ярким синим цветом. Максимум спектра флуоресценции з щелочной среде лежит при 440 ммк, в нейтральной и кислой - при 490 ммк. [21]
Все разобранные случаи гашения флуоресценции посторонними веществами не сопровождаются изменением свойств люмине-сцирующей молекулы. [22]
Уже отмеченный эффект гашения флуоресценции 2 - ( о-оксифе-нил) - бензоксазола в присутствии меди ( см. стр. Было показано, что 2 - ( о-оксифенил) - бензоксазол в кислой, нейтральной и слабощелочной средах флуоресцирует зеленым цветом, а в сильнощелочной-ярким синим цветом. Максимум спектра флуоресценции в щелочной среде лежит при 440 ммк, в нейтральной и кислой - при 490 ммк. [23]
Интересно отметить, что гашение флуоресценции флуорексона начинается с диссоциации 6-гидроксила. Поэтому нельзя согласиться с мнением Эггерса [7], что причиной флуоресценции флуоресцирующих комплексонов в кислой среде является образование водородной связи имина с фенильным кислородом, так как при диссоциации 6-гидроксила уже начинается гашение флуоресценции, несмотря на наличие водородной связи. [24]
Следует отметить, что гашение флуоресценции соединений XIX - XXIII - производных 2 2 -дифенилдиамина наблюдается в присутствии большего числа катионов ( Cu2, Со2, Ni2, Cd2 Mn2, РЬ2, Zn2), чем соединений XI-XVIII - производных 4 4 -ди-фенилдиамина. Это является, вероятно, как и у комплексона XVIII, следствием повышенной комплексообразующей способности соединений XIX-XXIII по сравнению с XI-XVIII; действительно, в комплексонах на основе бензидина ( XI-XVIII) иминодиацетат-ные группировки значительно удалены одна от другой; наиболее вероятно в этих случаях образование комплекса с открытой структурой, в которой металл координирован с одной хелатообразующей группой. [25]
Следует отметить, что гашение флуоресценции соединений XIX - XXIII - производных 2 2 -дифенилдиамина наблюдается в присутствии большего числа катионов ( Cu2, Co2, Ni2, Cd2 Mn2, РЬ2, Zn2), чем соединений XI-XVIII - производных 4 4 -ди-фенилдиамина. Это является, вероятно, как и у комплексона XVIII, следствием повышенной комплексообразующей способности соединений XIX-XXIII по сравнению с XI-XVIII; действительно, в комплексонах на основе бензидина ( XI-XVIII) иминодиацетат-ные группировки значительно удалены одна от другой; наиболее вероятно в этих случаях образование комплекса с открытой структурой, в которой металл координирован с одной хелатообразующей группой. [26]
В присутствии кобальта скорость гашения флуоресценции са-лицилфлуорона значительно увеличивается. При изучении кинетики этого процесса замечены две стадии окисления реагента. Скорость первой стадии зависит от концентрации кобальта, концентрации перекиси водорода, рН, ионной силы и температуры раствора. Скорость второй стадии зависит от рН и температуры раствора, но не зависит от ионной силы, концентрации перекиси водорода ( вплоть до 5 9 - 10 - 4 М) и концентрации кобальта. [27]
Одна из первых теорий гашения флуоресценции органических веществ примесями, разработанная Вавиловым79, основывалась на предположении, что гашение при соударениях зависит от числа соударений z между молекулами. В жидкости, особенно вязкой, две столкнувшиеся молекулы могут испытать ряд повторных соударений, прежде чем они разойдутся. В тех случаях, когда вероятность тушения при соударении очень велика, учитываются только лишь первые соударения, а если эта вероятность мала, то учитываются и повторные. [28]
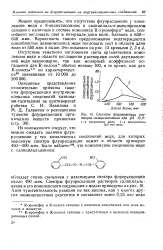 |
Спектры флуоресценции растворов салицилальазина при рН 12 0. [29] |
Описанные представления относительно причины гашения флуоресценции внутриком-плексных соединений катионами-гасителями не противоречат работам С. И. Вавилова и М. Д. Галанина о резонансном тушении флуоресценции органических веществ примесями ( стр. [30]
Страницы: 1 2 3 4